|
L&M-6-2014
>
Der Wahrnehmung von Nahrungsfetten auf der Zunge liegt ein komplexes Zusammenspiel von Rezeptoren und Lipasen zu Grunde
Der Wahrnehmung von Nahrungsfetten auf der Zunge liegt ein komplexes Zusammenspiel von Rezeptoren und Lipasen zu GrundeGeliebt und gehasst – die KalorienbombeFette als energiereichste Makronährstoffe spielen eine fundamentale Rolle in unserer täglichen Ernährung. Dabei beruht der Mechanismus der geschmacklichen Wahrnehmung von Fettbestandteilen auf einem fein abgestimmten Zusammenspiel von Rezeptoren und lipolytischen Enzymen. Während die Rezeptoren die Erkennung freier langkettiger Fettsäuren ermöglichen, haben die Lipasen die Aufgabe, diese aus den Nahrungsfetten freizusetzen. Unser Geschmackssinn erlaubt die sekundenschnelle Prüfung der Bekömmlichkeit von Nahrung, bevor wir diese verschlucken und unserem Organismus zuführen. Wir werden darüber informiert, ob die konsumierte Nahrung genügend Energie zur Verfügung stellt, um unseren Körper ausreichend zu versorgen, ob unser Salzhaushalt aufrechterhalten werden kann oder ob sogar schädliche Bestandteile den Verzehr der Speisen als nicht ratsam erscheinen lassen. All diese Informationen erreichen unser Gehirn, wo sie einzigartige Sinneseindrücke hervorrufen, die wir als die Grundgeschmacksarten süß, sauer, salzig, umami (wohl schmeckend, herzhaft) und bitter kennen (Abb.1) [1].
Abb.1 Unsere Geschmackswahrnehmung beruht auf den Qualitäten bitter, salzig, sauer, süß und umami (herzhaft). Der Frage, ob auch die gustatorische Wahrnehmung von Fetten zu den grundlegenden, eigenständigen Geschmacksrichtungen zählt, wollen wir mit unserer Forschung auf den Grund gehen. (Bild: © Nadine Voigt Wikimedia Commons Lizenz CC BY 3.0)
Ein stark saurer und insbesondere ein bitterer Geschmack führt zur Abneigung und hält uns sowohl von der bedenklichen Aufnahme unreifer oder verdorbener Lebensmittel als auch von Giftstoffen ab. Wir müssen stets eine gewisse Menge an Kochsalz zu uns nehmen, um ausscheidungsbedingte Verluste auszugleichen, jedoch nicht zu viel, weswegen wir salzig konzentrationsabhängig als angenehm oder unangenehm empfinden können. Im Gegensatz zu den oben genannten Grundgeschmacksarten bevorzugen wir süße und herzhaft (umami) schmeckende Lebensmittel mit großer, manchmal zu großer, Hingabe. Aus evolutionärer Sicht ist dies auch allzu verständlich, weisen uns diese Geschmacksqualitäten doch auf die Anwesenheit wichtiger Energieträger wie Kohlenhydrate und Proteine hin. Erkannt werden diese Makronährstoffe anhand ihrer Grundbausteine, den Mono- und Disacchariden im Falle des Süßgeschmacks sowie der Aminosäure L-Glutaminsäure im Falle des Umamigeschmacks. Mono- und Disaccharide sowie L-Glutaminsäure kommen in Lebensmitteln nicht nur als Bestandteile von Kohlenhydraten und Proteinen, sondern auch in freier Form vor. Diese Grundbausteine aktivieren spezialisierte Rezeptormoleküle auf den im Mund befindlichen Geschmacksknospen (Abb.2) und lösen dadurch Signale aus, die letztendlich zur Wahrnehmung von Süße bzw. Herzhaftigkeit führen. Während die geschmackliche Wahrnehmung der zwei Makronährstoffe Kohlenhydrat und Protein vergleichsweise gut untersucht ist, steckt die Erforschung der Wahrnehmung des dritten und energetisch bedeutsamsten Makronährstoffes, der Nahrungsfette, noch in den Kinderschuhen, eine Lücke, die wir mit unseren Arbeiten schließen wollen.
Abb.2 Geschmacksstimuli werden auf der gesamten menschlichen Zunge detektiert. Dies findet in spezialisierten Organen, den Geschmackspapillen statt. Die Geschmacksknospen in diesen Papillen setzen sich aus spezialisierten Zellen zusammen, die Geschmacksrezeptoren exprimieren und die Geschmacksinformation über die Anbindung an Nervenzellen an gustatorische Zentren im Gehirn weiterleiten (2a). Geschmacksknospen finden sich besonders zahlreich im Epithel der Wallpapillengräben. Hier münden ebenfalls die Drüsengänge der kleinen Speicheldrüsen (Von-Ebner-Drüsen) und sekretieren Enzyme, die in der Lage sind, geschmacksaktive Moleküle aus komplexen Nährstoffen freizusetzen. 16µm Gefrierschnitt nach H&E-Färbung (2b). (Bild: © Jonas Töle Wikimedia Commons Lizenz CC0 (gemeinfrei))
Die Wahrnehmung von Nahrungsfetten auf der Zunge Über viele Jahre herrschte die Meinung vor, dass die Wahrnehmung von Nahrungsfetten weitgehend auf ein charakteristisches Mundgefühl (mechanosensorische Wahrnehmung, Texturerkennung), ihre geruchliche Erkennung sowie vom Verdauungssystem ausgelöste Reize zurückgeht [2]. Eine Reihe tierexperimenteller Studien, bei denen die oben genannten Wahrnehmungswege blockiert wurden, führte jedoch zur Erkenntnis, dass auch der Geschmackssinn einen bedeutenden Beitrag bei der Erkennung von Nahrungsfetten leistet. Tatsächlich konnte gezeigt werden, dass nicht die Fette selbst, sondern, ähnlich wie beim Süß- und Umamigeschmack, Grundbausteine der Nahrungsmoleküle, nämlich die freien langkettigen Fettsäuren (Abb.4), Hauptauslöser der Fettwahrnehmung in der Mundhöhle von Nagetieren darstellen. Mehr noch, durch die Analyse genetisch veränderter Mäuse und die Durchführung physiologischer Experimente konnte eine Reihe potenzieller Rezeptormoleküle für die geschmackliche Wahrnehmung von Nahrungsfettbestandteilen identifiziert werden wie z.B. das Transportprotein CD36, der Kaliumionenkanal DRK sowie die G-Protein-gekoppelten Rezeptoren GPR40 und GPR120 [3,4]. Verglichen mit der Datenfülle aus Untersuchungen an Nagetieren war die Datenlage beim Menschen bis vor Kurzem eher als spärlich zu betrachten, ein Umstand, den wir zusammen mit unseren Kollegen des Lehrstuhls für Lebensmittelchemie und molekulare Sensorik der TU München im Rahmen DFG-geförderter Projekte ändern wollten. Unsere Arbeiten zeigen, dass auch der Mensch den GPR120, einen der oben aufgeführten Kandidatenrezeptoren für die Erkennung von Nahrungsfettbestandteilen, auf der Zunge exprimiert (Abb.3a) und dass die Aktivierung dieses Rezeptors durch langkettige freie Fettsäuren wie z.B. Ölsäure in vitro im Einklang mit sensorischen Untersuchungen beim Menschen steht (Tab.) [5]. Darüber hinaus zeigte sich auch, dass die untersuchten Fettsäuren unterschiedlicher Kettenlänge bei den menschlichen Probanden trotz des Einsatzes von Nasenklammern und der Maskierung der Textur von Kontroll- und Versuchslösungen eine als „fettig“ beschriebene Wahrnehmung auslösten. Dies traf jedoch nur für niedrige Konzentrationen langkettiger Fettsäuren zu, kurz- und mittelkettige Fettsäuren sowie hohe Konzentrationen langkettiger Fettsäuren wurden hingegen als „kratzig“ beschrieben. Interessanterweise ist das Hervorrufen eines „fettigen“ Geschmackseindruckes von der gleichzeitigen Verkostung einer freien langkettigen Fettsäure und eines Einbettungsmaterials mit fettähnlicher Beschaffenheit abhängig, was darauf hindeutet, dass Berührungsreize und gustatorische Erkennungsmechanismen eine Rolle spielen [5].
Tab. Die gustatorische Wahrnehmung von Fettsäuren und Triacylglyceriden
Die Bedeutung lipolytischer Enzyme für die Fettwahrnehmung Die mengenmäßig bedeutendste Komponente pflanzlicher Nahrungsfette sind nicht die freien Fettsäuren, sondern die Triacylglyceride, in denen jeweils drei Fettsäuremoleküle mit einem Glycerinmolekül verbunden sind (Abb.4). Unser nächstes Ziel war es daher zu ergründen, ob auch Triacylglyceride eine fettige Wahrnehmung bei menschlichen Probanden hervorrufen und der von uns auf der menschlichen Zunge gefundene Rezeptor GPR120 auf diese Verbindungen reagiert. Es zeigte sich, dass Trioleat – drei glyceringebundene Ölsäurereste – bei menschlichen Probanden einen als „fettig“ klassifizierten Eindruck hervorrief und im Gegensatz zur freien Ölsäure in höheren Konzentrationen nicht als „kratzig“ beschrieben wurde (Tab.). Jedoch konnte der Rezeptor GPR120 in einem speziellen Testverfahren nicht mit Trioleat aktiviert werden (Abb.3b) [6]. Somit ergab sich das Problem, entweder einen weiteren Rezeptor finden zu müssen, der durch Triacylglyceride aktiviert wird, oder einen Mechanismus nachzuweisen, der die Abspaltung freier Fettsäuren aus Triacylglyceriden erklären kann, die dann den GPR120-Rezeptor aktivieren. In Nagetieren konnte bereits eine Lipase identifiziert werden, die im Zungengewebe hergestellt wird und gezielt in der unmittelbaren Umgebung von Geschmacksknospen sekretiert wird. Die Blockierung der Aktivität dieser Lipase mit dem Inhibitor Orlistat reduzierte die zuvor beobachtete Vorliebe für den Geschmack von Triacylglyceriden dramatisch [7]. Im Gegensatz zu den Nagetieren, bei denen das Vorkommen und die Aktivität dieses auch als linguale Lipase bezeichneten Enzyms gut dokumentiert sind, findet man beim Menschen die höchste Expression dieses Enzyms in den Zellen der Magenschleimhaut (daher ist das gleiche Enzym beim Menschen als gastrische Lipase bekannt), aber nicht auf der Zunge [8]. Vorausgegangene Befunde zur lipolytischen Aktivität des menschlichen Speichels und zur Expression der lingualen Lipase zeichneten ein sehr heterogenes Bild [8,9]. Unsere eigenen Experimente haben nun gezeigt, dass das Gen für die linguale/gastrische Lipase (LIPF) überhaupt nicht auf der Zunge exprimiert wird und somit für die Freisetzung von Fettsäuren aus Triacylglyceriden im Mundraum nicht in Betracht gezogen werden kann (Abb.3a) [6]. Wie können dann also die zur Fettwahrnehmung notwendigen Fettsäuren entstehen? Um dies zu ergründen, haben wir untersucht, ob andere Lipasen aus derselben Genfamilie die Rolle der lingualen/gastrischen Lipase beim Menschen übernehmen könnten. In der Tat konnten wir die Expression von drei Lipasen – LIPK, LIPM, LIPN –, die bislang nicht mit dem Geschmackssystem in Verbindung gebracht wurden, in den kleinen Speicheldrüsen der menschlichen Zunge nachweisen (Abb.3a). Diese kleinen Speicheldrüsen sondern ihre Sekrete direkt in die Gräben der Wall- und Blätterpapillen ab, die mit den Geschmacksrezeptorzellen ausgekleidet sind. Die dort freigesetzten Lipasen könnten so direkt vor Ort Fettsäuren aus den Nahrungsfetten abspalten und dem GPR120-Rezeptor zugänglich machen. Sensorische Experimente unterstützen dieses Szenario, da auch in menschlichen Probanden die Wahrnehmung von Triacylglyceriden als „fettig“ unterdrückt werden kann, wenn gleichzeitig ein Lipaseinhibitor bei der Verkostung verwendet wird.
Abb.3 Im Rahmen unserer Untersuchungen zur gustatorischen Wahrnehmung von Fettsäuren und Triacylglyceriden konnten wir mithilfe von RT-PCR, Immunhisto- chemie und In-situ-Hybridisierung die Expression des fettsäuresensitiven Rezeptors GPR120 und einer Reihe Triacylglycerid-spaltender, sekretorischer Lipasen (bspw. LIPK) in den Geschmacksknospen humaner Wallpapillen bzw. den Von-Ebner-Speicheldrüsen zeigen. Pfeile weisen auf ausgewählte positive Zellen hin. bp: Basenpaare. M: DNA-Marker (3a). In zellbasierten In-vitro-Assays zeigte sich die spezifische Aktivierung des GPR120 durch langkettige Fettsäuren, nicht jedoch durch das entsprechende Triacylglycerid (3b). (B: Foto zur Verfügung gestellt von Stephan Born, Nuthetal)
Fettig – die sechste Grundgeschmacksqualität?
Die Frage, ob es sich bei der Wahrnehmung von Nahrungsfetten bei Säugetieren um eine Geschmackswahrnehmung im engeren Sinne handelt, kann zum jetzigen Zeitpunkt nicht abschließend beantwortet werden [10]. Ähnlich wie bei der fünften Grundgeschmacksart, umami, deren Anerkennung 75 Jahre lang nach Einführung in die wissenschaftliche Literatur kontrovers diskutiert wurde, müssen zahlreiche Voraussetzungen erfüllt werden. Ein wichtiger, noch ausstehender Schritt auf diesem Weg ist die Identifizierung einer eigenständigen Rezeptorzell-
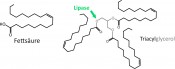
Abb.4 Struktur von freier Fettsäure und Triacylglycerol. Triacylglycerole sind Ester aus Glycerol und drei Fettsäuren. Lipasen spalten Fettsäuren aus Triacylglyceriden durch Hydrolyse der Esterbindung (Pfeil).
Wie auch immer diese Frage letztendlich beantwortet werden wird, es bleibt zu hoffen, dass es der Forschergemeinschaft schneller als im Falle des Umamigeschmacks gelingt, überzeugende Antworten zu finden. Literatur
[1] Behrens, M., Voigt, A. & Meyerhof, W. (2013) Ernährungs Umschau 60, 124–131 Bild: © panthermedia.net| yeko |
L&M 6 / 2014
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Die Autoren:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |