|
Biofilmanalyse in der Getränke- und Lebensmittelindustrie via Next Generation Sequencing
Biofilmanalyse in der Getränke- und Lebensmittelindustrie via Next Generation SequencingDie Sequenz im BierDie Entstehung von Biofilmen ist ein ernstzunehmendes Problem in der Getränke- und Lebensmittelindustrie. Nahezu jede Produktionsstätte weist kritische Bereiche (Schwachpunkte) auf, die ihre Bildung begünstigen. Biofilme sind ein Indiz für nicht greifende Reinigungsmaßnahmen. Sie mindern die Produktqualität und im schlimmsten Fall enthalten sie gesundheitsschädliche Keime. Wer sich davor schützen möchte, sollte im Vorfeld klären, welches Keimspektrum in der Produktionsstätte vorliegt. Wie entstehen Biofilme? Biofilme sind mikrobielle Lebensgemeinschaften, die sich aus Bakterien und Pilzen zusammensetzen können. Induktions-, Akkumulations- und Existenzphase sind die drei Phasen der Entstehung und Ausbildung eines Biofilms [1,2]. Die Induktionsphase beginnt mit der zufälligen Ansiedlung von Mikroorganismen an einer feuchten Grenzfläche. Die Mikroorganismen vermehren sich und produzieren dort eine extrazelluläre polymere Substanz (EPS), die nach Kontakt mit Flüssigkeit ein Hydrogel bildet. Die daraus resultierende Schleimschicht bietet den Mikroorganismen einen besseren Halt und schützt sie gleichzeitig vor äußeren Einflüssen. In der Akkumulationsphase wird die Schleimschicht dann von weiteren Keimen besiedelt, die sich dort vermehren und flächenmäßig als Film ausbreiten. Im späteren Stadium der Akkumulationsphase wachsen die Biofilme dann auch mehrschichtig auf und bilden komplexe dreidimensionale Strukturen. Von der Existenzphase spricht man, wenn ein Biofilm voll ausgereift ist. Der Biofilm kann sich jetzt nur noch begrenzt ausdehnen, da sich ein Gleichgewicht zwischen Zuwachs und Abbau von Biofilmmaterial eingestellt hat. Auch in der Existenzphase sind Biofilme sehr dynamische biologische Systeme. Es wird kontinuierlich neue Biomasse aufgebaut, es lösen sich aber auch regelmäßig ganze Teile eines Biofilms, die dann zu Produktverunreinigungen führen können. Biofilmanalyse mit Kulturverfahren Für die Untersuchung von Biofilmen wird eine Vielzahl optischer und spektroskopischer Verfahren herangezogen. Aufgrund hoher Geräte- und Untersuchungskosten sind sie derzeit jedoch vorwiegend wissenschaftlichen Zwecken vorbehalten. Den höchsten Stellenwert wird immer noch den kulturellen Analysen eingeräumt. Mit der entsprechenden Ausrüstung können sie in jedem Betrieb durchgeführt werden. Jedoch besteht der Nachteil eines enormen Arbeitsaufwandes, selbst wenn nur die Hauptbestandteile eines Biofilms bestimmt werden. Schnell kommen mehrere Dutzend Kulturplatten und Flüssigkulturen zusammen, die dann sehr zeitaufwändig mikroskopisch oder biochemisch zu untersuchen sind. Zusätzliche Hilfsmittel wie die MALDI-TOF-Analyse oder Sanger-Sequenzierung sind zwar mittlerweile in der Routinediagnostik einiger Labore angekommen, aber auch diese Methoden sind eher für die Analyse kleiner Probenserien gedacht. Hinzu kommt, dass Biofilme „Schläfer-Bakterien“ enthalten, die zwar lebensfähig sind, aber in der klassischen Kultur nicht angereichert werden können. Diese VBNC-Formen (Viable but not culturable) stellen ihre Stoffwechselaktivität nahezu vollständig ein, können aber jederzeit wieder reaktiviert werden. Neue Ansätze in der Biofilmanalytik Eine gute Alternative zu den Kulturverfahren stellen Mikrobiomanalysen dar, die eine direkte Analyse der Biofilme ermöglichen. Mikrobiomanalysen werden derzeit vorwiegend in wissenschaftlichen Einrichtungen durchgeführt. Sie bieten nicht nur neue Einblicke in die komplexe Welt der Mikroorganismen, sondern haben daneben ein gewaltiges Potenzial für die Identifizierung und Entwicklung neuer biotechnologischer oder pharmazeutischer Produkte [3]. Als Mikrobiom wird die Gesamtheit der genetischen Information aller Mikroorganismen in einer biologischen Lebensgemeinschaft bezeichnet. Das primäre Ziel einer Mikrobiomanalyse besteht darin, diese Informationen möglichst vollständig zu extrahieren. Mikrobiomanalysen werden mit einer Hochdurchsatz-Sequenzierung (Next Generation Sequencing) durchgeführt, die mehrere tausend Sequenzinformationen in einer einzelnen Untersuchung generieren kann (Abb.1). Die erhaltenen Sequenzen sind wie ein genetischer Fingerabdruck und können mithilfe von Datenbanken den jeweiligen Bakterien- bzw. Pilzgruppen zugeordnet werden. Die Anzahl identischer Sequenzen gibt zusätzlich Auskunft darüber, wie häufig die jeweiligen Mikroorganismen in einer Probe vertreten sind. Aufgrund der Kosten, die bei der Nutzung der Next-Generation-Sequencing-Technologie anfallen, spielen Mikrobiomanalysen immer noch eine untergeordnete Rolle in der Routineanalytik. Mittlerweile stehen aber günstige Geräte zur Verfügung, sodass diese Analysen auch für spezifische Fragestellungen in der Lebensmittelindustrie infrage kommen.
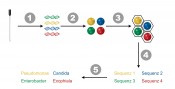
Abb.1 Mikrobiomanalyse von Biofilmen und Next Generation Sequencing. In den letzten Jahren wurden viele neue Verfahren der Hochdurchsatzsequenzierung entwickelt, die sich unter dem Begriff Next Generation Sequencing (NGS) zusammenfassen lassen [4]. Sie beruhen alle auf der Idee der massiven parallelen Sequenzierung von DNA-Fragmenten in einem einzigen Sequenzierlauf. Zunächst in der Forschung insbesondere für die Sequenzierung ganzer Bakteriengenome eingesetzt, hat die Anwendung von NGS mittlerweile das gesamte Feld der Molekularbiologie revolutioniert. Bei den Mikrobiomanalysen hat sich ein Sequenzierverfahren durchgesetzt, das mit den GS FLX- oder GS Junior-Systemen der Firma 454 Life Science durchgeführt wird [5] (siehe Infokasten).
Biofilme und ihre Bestandteile Der durchschnittliche Biofilm in einer Produktionsstätte ist weniger komplex, als man vermuten mag. Eine von uns durchgeführte Pilot-Studie zeigt, dass Biofilme hauptsächlich von wenigen Bakterien bzw. Pilzen dominiert werden und zusätzlich eine große Anzahl unterschiedlicher Mikroorganismen in geringer Abundanz enthalten (Abb.2). Dieses Verteilungsmuster ist reproduzierbar und findet sich in allen bisher untersuchten Biofilmen. Gravierende Unterschiede findet man jedoch in der Zusammensetzung: Da gleicht kein Biofilm dem anderen. Innerhalb einer Produktionskette entstehen Biofilme meist unabhängig voneinander und können ein völlig unterschiedliches Bakterien- und Pilzspektrum aufweisen. Die Analyse eines einzelnen Biofilms reicht daher nicht aus, um ein vollständiges Bild zu erhalten. Für aussagekräftige Ergebnisse ist es wichtig, alle kritischen Bereiche einer Produktionskette zu untersuchen (Tab.1). Erfahrungsgemäß werden für die Analyse eines Biofilms lediglich drei- bis viertausend Sequenzen benötigt. Das bietet die Möglichkeit, mehrere Biofilme gleichzeitig zu analysieren, da alle Geräte, die für das Next Generation Sequencing eingesetzt werden, ein Vielfaches dieser Datenmenge generieren können. Die von „Das Bierlabor“ verwendeten GS Junior-Systeme produzieren bei jeder Untersuchung so viele Sequenzdaten, dass gleichzeitig acht Biofilme auf Bakterien und Pilze untersucht werden können. Damit kann ein umfassendes Bild von einer Produktstraße oder sogar des gesamten Betriebes erstellt werden. Ausgehend von den erhaltenen Ergebnissen können dann geeignete Reinigungsstrategien für die jeweiligen Teilbereiche ermittelt werden. Zusätzlich erhält man einen guten Überblick, mit welchen Produktkontaminationen an den jeweiligen Stellen zu rechnen ist.
Abb.2 Auswertung einer Biofilmanalyse. Die Mikrobiomanalyse eines Biofilms liefert in der Regel eine große Anzahl verschiedener Mikroorganismen mit unterschiedlicher Abundanz. Um den Befund einer Biofilmanalyse übersichtlich zu gestalten, werden die häufigsten Bakterien und Pilze grafisch dargestellt und alle weiteren Mikroorganismen tabellarisch aufgeführt. Insgesamt konnten in dieser Analyse 235 verschiedene Bakterien und 485 Pilzarten nachgewiesen werden.
Tab.1 Biofilmanalyse einer Brauerei. Innerhalb einer Produktionskette entstehen Biofilme meistens unabhängig voneinander und können daher völlig unterschiedliche Bakterien- und Pilzspektren aufweisen. Die Tabelle zeigt die Zusammensetzung von Biofilmen, die an unterschiedlichen Punkten einer Füllerstraße gesammelt wurden. Alle Biofilme des untersuchten Betriebes unterscheiden sich hinsichtlich ihres Bakterien- und Pilzspektrums. Aussagekräftige Ergebnisse können nur mit der Untersuchung aller kritischen Bereiche erhalten werden.
Mikrobiomanalysen – Yin und Yang Die Untersuchung von Biofilmen mit einer Mikrobiomanalyse bietet viele Vorteile. Da die Methode keine kulturelle Anreicherung benötigt, entfällt der aufwändige Spezialtransport der Proben. Für die Analyse werden lediglich Abstriche mit Biofilmmaterial benötigt, die bequem verschickt werden können. Weiterhin ist es möglich, die Abstriche nach der Probennahme für längere Zeit in einem Kühl- oder Gefrierschrank zu lagern, ohne dass die Qualität der Analyse beeinträchtigt wird. Damit lassen sich auch Verlaufskontrollen über mehrere Tage oder Wochen problemlos durchführen. Den größten Vorteil bietet jedoch die hohe analytische Sensitivität der Methode. Die Untersuchung liefert auch dann aussagekräftige Ergebnisse, wenn der Biofilm mit bloßem Auge noch gar nicht sichtbar ist. Somit lassen sich Probleme früh erkennen und Produktschäden vermeiden. Hinsichtlich der Untersuchungsdauer kann die Methode ebenfalls punkten. Die Ergebnisse einer Mikrobiom-Analyse liegen in der Regel nach fünf bis sieben Werktagen vor, sodass dringend benötigte Ergebnisse schnell zur Verfügung stehen. Aber jede Medaille hat zwei Seiten: Wer auf die Mikrobiomanalysen setzt, wird auch mit Mikroorganismen konfrontiert, die in keinem Handbuch der Getränke- und Lebensmittelindustrie zu finden sind. Derzeit vermuten Experten, dass mehr als 99% aller existierenden Mikroorganismen nicht kultivierbar und daher mit mikrobiologischen Methoden auch nicht identifizierbar sind. Ein Teil dieser Mikroorganismen wird sich in Biofilmen nachweisen lassen und macht die Risikobewertung eines Befundes anspruchsvoller. Daher sollten die Ergebnisse einer Mikrobiomanalyse immer in einem multidisziplinären Team aus internen und externen Fachleuten diskutiert werden. Dagegen bietet der Nachweis bisher unbekannter Mikroorganismen die Chance, neue Strategien zur Bekämpfung von Biofilmen zu entwickeln. Ausblick Analysen dieser Größenordnung ersetzen natürlich nicht die tägliche Stichprobe. Denn die klassische Mikrobiologie ist und bleibt ein essenzieller Bestandteil der täglichen Laborroutine. Aber: Mikrobiomanalysen von Biofilmen können – sofern sie richtig eingesetzt werden – Schwachpunkte innerhalb der Produktion überwachen und rechtzeitig wichtige Informationen über neue Kontaminationsquellen liefern. Darüber hinaus sind Mikrobiomanalysen nicht auf die Untersuchung von Biofilmen beschränkt. Vielmehr können sie in allen Bereichen eingesetzt werden, in denen mikrobielle Verunreinigungen eine Rolle spielen.
Literatur Bild: © istockphoto.com| Lauri Patterson |
L&M 2 / 2015
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |