|
Forscher
>
Prof. Dr. Fritz Boege
>
Die Haut als Indikator des biologischen Alters
Die Haut als Indikator des biologischen AltersNicht nur eine Frage der KosmetikDer morgendliche Blick in den Spiegel zeigt Falten, Pigmentflecken, Säcke unter den Augen, erweiterte Äderchen. Das ist unschön. Ist es auch besorgniserregend? Wie steht es im Inneren? Sagt uns die Haut, wie stark der Körper insgesamt gealtert ist? Kirchenvater Augustinus (354–430) bezeichnete den menschlichen Körper als den Bruder Esel, der eine unsterbliche Seele mühsam ins Jenseits schleppt. Heute steht uns dieser Bruder Esel oftmals näher als das Jenseits. Wir wollen, dass unser Bruder Esel möglichst wenig Mühe hat und möglichst lange durchhält. Wir wollen erfolgreich altern. Worin besteht erfolgreiches Altern? Die genetische Grundlage bestimmt die maximale Lebensspanne und damit den Rahmen dessen, was bestenfalls möglich ist. Die Lebensführung entscheidet, wie dieser Rahmen genutzt wird. Wer schnell altert, hat ein hohes Risiko, gebrechlich zu werden. Wer langsam altert, hat bessere Chancen, vorher eines zufälligen Todes aufgrund einer Infektion, eines Unfalls oder dergleichen zu sterben. Das nennen wir erfolgreich altern: Jung sterben, nachdem man lange gelebt hat (Abb.1).
Abb.1 Erfolgreiches Altern und der Zusammenhang zwischen maximaler Lebenspanne, mittlerer Lebenserwartung und Altersgebrechlichkeit. Bei erfolgreichen Lebensläufen (grün) liegen mittlere Lebenserwartung und maximale Lebenspanne nahe beieinander und der Schnittpunkt mit der kumulativen Wahrscheinlichkeit eines zufälligen, alterungsunabhängigen Todes (roter Kreis auf gestrichelter Linie) liegt außerhalb des Erlebnishorizonts der Altersgebrechlichkeit (graue Fläche). Bei unerfolgreichen Lebensläufen (rot) ist die mittlere Lebenserwartung sehr viel kürzer als die maximale Lebenspanne. Der Schnittpunkt mit der kumulativen Wahrscheinlichkeit eines zufälligen, alterungsunabhängigen Todes kommt innerhalb des Erlebnishorizonts der Altersgebrechlichkeit zu liegen.
Wie kann man erfolgreiches Altern fördern? Wenn man die maximale Lebensspanne verlängert, steigt die Wahrscheinlichkeit eines alterungsunabhängigen Todes. Heute sterben in Deutschland weit mehr als die Hälfte der Menschen an Gebrechlichkeit oder altersassoziierten Erkrankungen. Bei vierfach längerer maximaler Lebensspanne würden wohl fast alle Todesfälle alterungsunabhängige Ursachen haben. Wir würden dann alle jung und gesund sterben. Eine schöne Vision. Die technische Umsetzung würde umfangreiche Eingriffe in die genetische Basis des Menschen erfordern. Das liegt in sehr weiter Ferne. Was bereits heute möglich ist: die gezielte Verbesserung des Alterungserfolgs im genetisch vorgegebenen Rahmen. Dies ist einerseits durch körperliche Aktivität und sparsame Ernährung, andererseits durch eine gezielte pharmakologische Intervention gegen alterungsrelevante Signal- und Stoffwechselwege möglich. Für den gezielten Einsatz antigeriatrischer Pharmaka (die es bereits gibt oder die gerade entwickelt werden), ist es allerdings notwendig festzustellen, wogegen interveniert werden muss, welche Signal- und Stoffwechselwege an der Beschleunigung des Alterungsprozesses im individuellen Fall tatsächlich beteiligt sind. Organtypische Alterungsszenarien Altern ist ein multifaktorieller Prozess, an dem viele Signal- und Stoffwechselwege beteiligt sind. Gruppierungen dieser molekularen Alterungsmechanismen wirken in typischen Alterungsabläufen zusammen. Man bezeichnet solche Gruppen als Alterungsmerkmale (Hallmarks of Aging, Abb.2) [1]. Davon kennen wir wenigstens neun verschiedene, die in einzelnen Organen und Geweben zu sehr unterschiedlichen Alterungsszenarien kombiniert sind: Gewebe mit hohem Zellumsatz sind grundsätzlich anderen Alterungsszenarien unterworfen als Organe mit geringem Zellumsatz, im Bewegungsapparat laufen andere Alterungsprozesse ab als im Verdauungssystem usw. Dabei dominieren jeweils einige wenige Prozesse in einigen wenigen Geweben den Zustand des Gesamtorganismus und bedingen dessen biologisches Alter. Diese gilt es zu identifizieren, um dann gezielt dagegen vorzugehen. Dafür benötigt man jedoch eine differenzierte Diagnostik.
Abb.2 Hallmarks of Aging: Das Schema zählt die neun Hallmarks oder Kennzeichen auf, nach denen die molekularen Alterungsprozesse auf dem derzeitigen Stand der Forschung klassifiziert werden (entnommen aus Literatur [1]).
Diagnostik des biologischen Alters Blut ist das klassische Probenmaterial der medizinischen Diagnostik. Tatsächlich zeigen fast alle gängigen im Blut erhobenen diagnostischen Parameter altersabhängige Veränderungen. Daneben kennt man reine Altersmarker, also Laborparameter, deren mittlere Wertlage über die gesamte Lebenspanne hinweg streng mit dem chronologischen Alter korreliert. Hierzu zählen bestimmte Signaturen der DNA-Methylierung, Asparagin/Aspartat-Isomere in langlebigen Plasmaproteinen und Veränderungen im Glykierungsmuster von Immunglobulinen. Solche Marker werden teilweise zu forensischen Zwecken eingesetzt, um z.B. das Berentungsdatum von anatolischen Gastarbeitern festzusetzen, deren Geburtsdatum unbekannt ist. Es ist jedoch fraglich ob das Blut als Transportmedium mit hohem Durchsatz und kurzer Komponentenhalbwertszeit geeignet ist, Divergenzen von biologischem und chronologischem Alter aufzudecken und die zugrundeliegenden Alterungsprozesse abzubilden, die in langlebigen Zell- und Organsystemen ablaufen. Streng genommen müsste eine solche Diagnostik in den betroffenen Organen selbst erfolgen, was jedoch nicht praktikabel ist. Es ist somit notwendig, ein geeignetes Indikatororgan nebst entsprechendem Probenmaterial für eine standardisierte Diagnostik des biologischen Alterungszustandes zu finden. Dieses Indikatororgan sollte die wesentlichen organbezogenen Alterungsszenarien repräsentieren. Das daraus abgeleitete Probenmaterial sollte in der medizinischen Regelversorgung handhabbar sein. Die Haut ist das einzige Organ, das allen diesen Anforderungen genügen kann. Die Haut als Indikatororgan Die Haut ist als Grenzflächenorgan ein wesentlicher Austragungsort der Auseinandersetzung des Körpers mit altmachenden Umwelteinflüssen und schon deshalb als Indikatororgan dieser Auseinandersetzung prädestiniert. Die Haut besitzt klar voneinander abgegrenzt ein proliferatives Kompartiment (die Epidermis) und ein non-proliferatives Kompartiment (die Dermis), und kann somit als Stellvertretermodell dieser beiden grundlegenden Gewebetypen und ihrer typischen Alterungsprozesse dienen (Abb.3). Die Haut ist das einzige Organ, bei dem der biologische Alterungszustand mit nichtinvasiven Methoden (Inspektion, physikalische Messungen) feststellt werden kann. Die Haut ist neben dem Blut das einzige Organ, dem mit vertretbarem Aufwand und Risiko im gesunden Menschen eine Biopsie entnommen werden kann. Aus Hautbiopsien können standardisierte primäre Gewebekulturen abgeleitet werden, in denen der Alterungszustand von Zellfunktionen beobachtet werden kann.
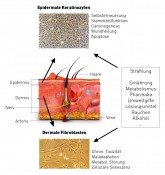
Abb.3 Hautkompartimente und daraus abgeleitete primäre Zellkulturmodelle. Die wesentlichen drei Schichten der Haut sind die Dermis, die Epidermis und die Subcutis. Die Epidermis bildet die Grenzschicht zur Umwelt und ist ein ständig proliferierender Zellverbund aus dem das Kulturmodell der Keratinozyten abgeleitet wird. Die Dermis (Lederhaut) sorgt für strukturelle Festigkeit und besteht im Wesentlichen aus Bindewebefasern und Fibroblasten. Fibroblasten teilen sich selten teilen und dienen als Kulturmodell langlebiger Gewebe. Äußere Triebfedern der Alterung induzieren in diesen beiden Zellmodellen unterschiedliche Alterungsprozesse, die als Indikatoren vergleichbarer Prozesse in inneren Organen dienen können. Quelle (Keratinozyten, Fibroblasten): www.bcp.fu
Nichtinvasive Diagnostik der biologischen Alterung Wir sind darauf geeicht, das biologische Alter eines Menschen intuitiv zu erfassen. Hierfür verwenden wir in erster Linie visuelle Informationen über Körperhaltung und -beweglichkeit sowie den Zustand der Haut und ihrer Anhangsorgane. In der Dermatologie wurde mit dem SKINEXA®-SCORE ein systematisches und präzises Werkzeug der visuellen Beurteilung des Hautalters etabliert, das den Status verschiedener Hautalterungsprozesse unterscheidet und dabei genetische und ethnische Unterschiede der Hauttypen berücksichtigt [2]. Mithilfe des SKINEXA-SCOREs kann eine beschleunigte Hautalterung aufgrund verschiedener umwelttoxischer Einflüsse erfasst werden und es gibt erste Hinweise, dass sich daraus Vorhersagen über den Alterungszustand anderer Organsysteme (Gehirn, Niere, Skelettmuskel) ableiten lassen, in denen ähnliche molekulare Alterungsprozesse ablaufen wie in der Haut. Ein weiterer, nichtinvasiv objektivierbarer Surrogat-Parameter des biologischen Alters ist die Autofluoreszenz der Haut, die aufgrund der Modifikation des dermalen Bindegewebes mit Glukosederivaten (sogenannten advanced glycosylation endproducts) mit zunehmendem Alter ansteigt (Abb.4). Dies korreliert stringent mit der Anreicherung von advanced glycosylation endproducts im Bindegewebe der Gefäßwände und erlaubt eine belastbare Vorhersage über die altersabhängige Gefäßversteifung, die ansonsten mit aufwendigen Doppleruntersuchungen der Pulswellenlaufgeschwindigkeit bestimmt wird [3]. Man geht davon aus, dass der Anstieg der Autofluoreszenz der Haut auch mit der Anreicherung von advanced glycosylation endproducts in anderen Bindegewebskompartimenten korreliert und deshalb auch Vorhersagen über den Alterungsprozess z.B. des Bewegungsapparates ermöglichen würde. Dies wurde jedoch noch nicht untersucht. Auch eine systematische Verknüpfung von SKINEXA-SCORE und Hautautofluoreszenz wurde noch nicht evaluiert. Hauthistologische Marker der biologischen Alterung Die Hautalterung ist durch eine Reihe charakteristischer histologischer Veränderungen gekennzeichnet: Abflachung der Epidermis, Verlust und Unordnung des dermalen Bindegewebes, vermehrte Gefäßeinsprossung, Abbau des subdermalen Fettgewebes, Zunahme entzündlicher Infiltrate. Einige dieser Veränderungen sind typisch für die durch Sonnenlicht angetriebene Komponente der Hautalterung, andere treten auch in gealterter Haut auf, die üblicherweise vor Licht geschützt ist. Ähnliche histologische Veränderungen treten auch in anderen gealterten Geweben auf. So findet in vielen stationären (nicht proliferierenden) Geweben mit dem Alter eine zunehmende Entzündungsreaktion mit Einsprossung von Gefäßen, vermehrter Freisetzung von Entzündungshormonen und Einwanderung von Entzündungszellen statt. Man nennt das InflammAging. Es steht zu vermuten dass die Ausprägung von histologischen Kennzeichen des InflammAging in lichtgeschützen Hautarealen mit dem Status dieses Alterungsprozesses in anderen Organen korreliert. Dies wurde jedoch noch nicht systematisch untersucht. Ein weiteres Kennzeichen der Alterung stationärer Gewebe ist die Anhäufung von DNS-Schadensmarken (phosphoryliertes Histon, yH2AX) und die chronische Aktivierung von DNS-Schadensreportern, die den Zellzyklus anhalten (p21/WAF1/CIP und p16INK4A). Dadurch wird zwar eine maligne Entartung der geschädigten Zellen verhindert, aber gleichzeitig ein irreversibler, quasi untoter Zustand erzeugt, den man zelluläre Seneszenz nennt. Es konnte nachgewiesen werden, dass seneszente Zellen die Alterung verschiedener Gewebe (Gehirn, Herz/Kreislaufsystem, Skelettmuskel) antreiben können, und man beobachtet eine Anreicherung der o.g. Seneszenzmarker in der Haut alter Menschen. Es liegt nahe zu vermuten, dass der Hautbefund mit dem Altersprozess in den inneren Organen und Geweben korreliert. Dies wurde jedoch noch nicht direkt untersucht.
Abb.4 Hautautofluoreszenz als Surrogatparameter des biologischen Gefäßalters. A) Mit dem Lebensalter steigt die Modifizierung des Kollagens der Gefäßwände Glukosederivaten (sog. Maillard-Reaktion). B) Die Collagenglykierung in den Gefäßwänden korreliert mit der Hautautofluoreszenz und C) mit der arteriellen Pulswellengeschwindigkeit. D) Somit korreliert die Hautautofluoreszenz mit der der arteriellen Pulswellengeschwindigkeit. E) Da die arterielle Pulswellengeschwindigkeit ein direktes Maß für die Alters- und Diabetes-assoziierte Versteifung der Gefäße ist, kann die Hautautofluoreszenz als Surrogatparameter für das biologische Gefäßalter dienen (Abbildung modifiziert nach Literatur [3]).
Ex-vivo-Analyse des Status von Alterungsprozessen in primären Hautzellen Viele Alterungsmerkmale und molekulare Alterungsmechanismen lassen sich nicht durch einen histologischen Schnappschuss fassen. Es handelt sich um diskrete quantitative Änderungen von zellbiologischen Funktionen, z.B. im Energiestoffwechsel, in der Nährstofferkennung und -verwertung, in der zirkadianen Regulation, in der Homöostase und Qualitätskontrolle von Proteinen oder in der Zell-Zell-Kommunikation. Solche diskreten Veränderungen können nur durch Funktionsmessung im Zellkulturmodell erfasst werden. Das wichtigste Arbeitspferd in der Aufklärung solcher altersassoziierter Veränderung von Zellfunktionen war über viele Jahrzehnte der dermale Fibroblast, der in standardisierten Verfahren aus Hautbiopsaten isoliert und in Kultur gehalten werden kann, ohne dass dafür eine maligne Transformierung notwendig ist (das nennt man Primärkultur). Bereits 1961 entdeckte Hayflick [4], dass diese Zellen in der Kultur spontan altern und schließlich aufhören, sich zu teilen, was 50 Jahre später auf die replikative Verkürzung der Chromosomenenden (Telomere) zurückgeführt wurde (unter anderem dafür erhielten Blackburn, Greider und Szostak 2009 den Nobelpreis für Physiologie). Auch viele andere Alterungsmerkmale lassen sich an in vitro gealterten dermalen Fibroblasten nachweisen. Nur einige wenige dieser Alterungsmerkmale findet man auch in dermalen Fibroblasten aus der Haut alter Menschen wieder, die in vivo gealtert sind und nach nur kurzer Primärkultur ex vivo analysiert werden [5]. Diese Altersmerkmale der Fibroblastenalterung ex vivo sind wahrscheinlich ein wichtiger prognostischer Parameter für den Stand vergleichbare Alterungsprozesse in inneren Organen und Geweben. So zeigen Fibroblasten aus der Haut 60- bis 70-jähriger Menschen eine markante Störung des Energiestoffwechsels und der Mitochondrienfunktion (Abb.5) [6], die auch in der Skelettmuskulatur wesentlich älterer Menschen auftritt und dort Muskelschwäche (Sarkopenie) auslöst, was schließlich in Immobilität und Gebrechlichkeit mündet. Es liegt nahe zu vermuten, dass die Störung im Energiestoffwechsel der Hautfibroblasten der vergleichbaren Störung in den Muskeln vorausläuft, diese vorhersagen und somit eine präventive Intervention gegen den Muskeldefekt begründen kann.
Abb.5 Störung des Energiestoffwechsels in alten Hautfibroblasten. Mit dem Lebensalter sinkt die zelluläre Mitochondriendichte (A). Weniger Mitochondrien leisten die gleiche Arbeit, weshalb der Sauerstoffverbrauch konstant bleibt (D). Jedoch steigt der Elektronendurchsatz durch die Atmungskette und es kommt zur vermehrten Produktion von Sauerstoffradikalen (B). Das Potenzial an der inneren Mitochondienmembran steigt an (C). Im Zuge der chronischen Überlastung sinkt schließlich die ATP-Produktion und der ADP/ATP-Quotient steigt an (modifiziert nach Literatur [6]).
Schlussbemerkung In den kommenden Jahren und Jahrzehnten wird eine gezielte medizinische Prävention und Intervention dafür sorgen können, dass wir erfolgreicher altern. Voraussetzung ist eine differenzierte Diagnostik des multifaktoriellen und heterogenen Alterungsgeschehens in den für die Alterssyndrome relevanten Organen und Geweben. Diese Diagnostik wird nicht allein auf konventioneller Analytik von Blutproben basieren können, weil sich im peripheren Blut das biologische Alter nicht zuverlässig abbildet. Es gibt eine Reihe von Hinweisen, dass die Hautalterung Vorhersagen über wesentliche Facetten des globalen biologischen Alters erlaubt. Die dafür notwendige Diagnostik setzt sich aus nichtinvasiven Messungen, histologischen Analysen und Ex-vivo-Zellmodellen zusammen. Diese Untersuchungen sind von Aufwand und Risiko her grundsätzlich für eine präventive Anwendung am gesunden Menschen geeignet.
Literatur Bilder: © istockphoto.com| grivina, 7 activestudio |
L&M 1 / 2015
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |