|
DNA übersteht den Wiedereintritt in die Erdatmosphäre
DNA übersteht den Wiedereintritt in die ErdatmosphäreIns Weltall und zurückDesoxyribonukleinsäure (engl. deoxyribonucleic acid, DNA) ist das Molekül des Lebens, das in allen Organismen und vielen Viren die Erbinformation trägt. Bei einem Experiment auf der Forschungsrakete TEXUS-49 konnten wir zeigen, dass ungeschützte DNA grundsätzlich den Eintritt in die Erdatmosphäre übersteht und nach Ankunft auf der Erde genetische Information weitergeben kann. Reger kosmischer Materialaustausch Unsere Erde reist nicht in einer isolierten „Box“ durch das All. Pro Jahr gelangen etwa 40.000 t extraterrestrisches Material in Form von kosmischem Staub und Meteoriten auf die Erde. Schätzungen rechnen mit über 4 Mrd. t Material allein vom Mars, das in der Geschichte des Sonnensystems auf die Erde gelangte, das allermeiste davon, ohne je hohen Temperaturen über 100°C ausgesetzt gewesen zu sein. Bei schnell in die Erdatmosphäre eintretenden Meteoriten muss die Gesteinsschicht nur 5?cm dick sein, damit sich das Innere auf nicht mehr als 121°C erhitzt [1], das bisher bekannte Maximum für thermophiles Leben [2]. Angesichts des regen Austausches kosmischen Materials zwischen Himmelskörpern drängt sich die Frage auf, ob auch Moleküle des Lebens oder lebende Organismen selbst auf Stäuben oder in Meteoriten auf die große kosmische Reise gehen. Erstaunlich widerstandsfähiges Leben Bausteine des Lebens wie Aminosäuren und Purinbasen, Bausteine der DNA, konnten in Meteoriten und in interstellaren Gaswolken außerhalb der Erde nachgewiesen werden [3]. Nicht nur die Bausteine des Lebens, auch Leben selbst kann erstaunlich widerstandsfähig sein. Leben kann unter extremen physikalischen und geochemischen Bedingungen existieren. Sehr hohe oder sehr tiefe Temperaturen, Strahlung, Druck, Vakuum, Austrocknung, hohe Salzkonzentrationen oder Säuren können vielen Lebensformen nichts anhaben [4]. Auf der EuTEF-Einrichtung (European Technology Exposure Facility) des Europäischen Columbus-Moduls der Internationalen Raumstation überlebten Mikroorganismen 1,5Jahre ungeschützt im freien Weltall. Polyextremophile Bakterien wie Deinococcus radiodurans ertragen Strahlendosen bis zu 10.000Gy, und das weitverbreitete Darmbakterium Escherichia coli wächst noch unter der 400.000-fachen Schwerkraft der Erde [5]. Leben kann unter den erstaunlichsten Bedingungen und in extremsten Umwelten existieren. Es könnte weiter verbreitet sein, als wir uns vorzustellen vermögen. Die Anzahl von erdähnlichen Planeten allein in unserer Galaxie, die in einer habitablen Zone liegen, schätzt das European Southern Observatory auf 10 Mrd. Biosignaturen zum Aufspüren von Leben Bei der Suche nach Leben werden Methoden zur Detektion von Biosignaturen eingesetzt. Unter Biosignaturen werden in der Astrobiologie Moleküle verstanden, die einen Hinweis auf gegenwärtiges oder früheres Leben liefern. Die Stabilität dieser Biosignaturen unter den Bedingungen des Weltraumes oder des Transportes zwischen Planeten ist daher eine wesentliche Grundfrage der Astrobiologie. DNA ist eine geeignete Biosignatur, da sie in allen lebenden Organismen den Speicher der Erbinformation repräsentiert und aufgrund des Nachweises ihrer Bausteine (Purinbasen) in Meteoriten und interstellaren Gaswolken eine universelle Bedeutung vermutet werden kann. Ein spontan erdachtes Zusatzexperiment März 2011, Esrange (European Space and Sounding Rocket Range) bei Kiruna, 150km nördlich des Polarkreises: Wir bereiten mit unserem Team ein Experiment auf der Höhenforschungsrakete TEXUS-49 vor. Als Gravitationsbiologen untersuchen wir auf Ebene des gesamten Genoms die Schwerkraftabhängigkeit der Genexpression. Dazu dienen speziell konstruierte, voll automatisierte Experimenteinheiten, die im Inneren der Nutzlast der zweistufigen TEXUS-Rakete ins All fliegen. Wir fragten uns, ob auch die Außenhülle nicht eine sinnvolle Testplattform für die Stabilität von Biosignaturen sein könnte. Wir sind keine Experten in Astrobiologie und planten daher zunächst einen vorsichtigen Vortest, einen einfachen Technologietest für die Machbarkeit der Nutzung von Höhenforschungsraketen für Stabilitätsstudien an Biosignaturen. Mögliches neues Anwendungsfeld für Forschungsraketen Experimente an Bord der Internationalen Raumstation (ISS) oder auf einem Forschungssatelliten sind aufgrund der geringen Flugsequenz, Kosten und Sicherheitsanforderungen sehr limitiert. Höhenforschungsraketen könnten eine geeignete Alternative zu diesen Plattformen darstellen, wenn die Auswirkungen von Schwerelosigkeit sowie des Durchtritts durch die Erdatmosphäre auf Materialien oder biologische Systeme untersucht werden soll. Basierend auf der Nutzlast-Raketenmotor-Konfiguration kann eine Mikrogravitationsdauer zwischen drei und dreizehn Minuten erzielt werden. Wir hatten die Idee, zusätzlich zu den im Innern der Nutzlast befindlichen Experimenten die Außenseite der Nutzlast für astrobiologische Untersuchungen einzusetzen und damit das mögliche Anwendungsspektrum von Forschungsraketen zu erweitern. In unserer technischen Pilotstudie testeten wir die Auswirkung des Verlassens und Wiedereintritts in die Erdatmosphäre auf die Stabilität von DNA. Plasmid-DNA als Modell-Biosignatur Für dieses Experiment wurde eine gut charakterisierte und häufig in der molekularbiologischen Forschung eingesetzte Plasmid-DNA (pEGFP-C3) als Modell-Biosignatur verwendet. Diese zirkuläre DNA trägt Abschnitte, die sowohl für das grün fluoreszierende Protein (GFP) als auch für das Resistenzgen Kanamycin kodieren. Die beiden Marker kommen in dieser Kombination nicht natürlich vor und sind deshalb nach dem experimentellen Flug im wiedergewonnenen Probenmaterial eindeutig zu identifizieren. Beide Marker können eingesetzt werden, die Funktionalität der DNA zu analysieren. In Bakterien oder eukaryote Zellen eingebracht, vermittelt ein intaktes, zirkuläres Plasmid eine Antibiotikaresistenz bzw. die Expression eines grün fluoreszierenden Proteins; die Zellen fangen an zu leuchten. Plasmid-DNA wurde in großen Mengen isoliert, in einer wässrigen salzhaltigen Lösung aufgenommen und zum Esrange Space Center in die Arktis gebracht. Bereit für die große Reise Auf der Außenseite der Nutzlast wurden 15 verschiedene Positionen für die Test-DNA ausgewählt und gründlich gereinigt. Danach wurde die in einem Salzpuffer gelöste DNA an zwölf Positionen zirkulär mit definiertem Abstand entweder direkt auf die Oberfläche der Nutzlast oder in die Vertiefungen von Schraubenköpfen aufgetragen, drei Proben wurden zusätzlich auf die Unterseite der Nutzlast aufgebracht (Abb.1). Die DNA wurde anschließend mit einem standardisierten Verfahren angetrocknet und bis zum Start mit einer Folie geschützt. Während des Countdowns wurden die Folien vollständig entfernt. Zusätzlich zu den 15 Proben wurde eine Positivkontrolle auf einer separaten Nutzlastaußenhülle aufgetragen, die nicht ins All geschossen wurde, und dort bis nach dem erfolgreichen Flug für insgesamt neun Tage belassen. Zusätzlich wurden an drei verschiedenen Positionen Negativkontrollen als Kontaminationskontrollen durchgeführt. Diese Positionen waren repräsentativ für die unterschiedlichen Applikationsorte (Oberfläche, Schraubenköpfe und Unterseite).
Abb.1 Auftragen von Plasmid-DNA auf der Außenseite der TEXUS-49 Nutzlast. DNA-Proben wurden in 12 Positionen (Abb.1a) auf der Außenseite des TEM (TEXUS Experiment Modul) EML aufgetragen. Die Proben 1-4 wurden zirkulär bei 0, 90, 180 und 270o direkt auf die Oberfläche der Nutzlast aufgetragen. Für das Auftragen der Proben 5–12 wurden Schraubenköpfe im Abstand von 90o ausgewählt (Querschnitt des TEM-EML, Abb.1cI). Die DNA-Proben 13–15 wurden an der Unterseite der Nutzlast, direkt auf der Oberfläche, aufgebracht (Abb.1cII). Für das Auftragen der DNA auf die Nutzlastoberfläche wurde der ausgewählte Bereich zuerst markiert, dann gereinigt und danach die DNA aufgetragen (Abb.1d). Die DNA-Proben 5–12 wurden direkt in die gesäuberten Vertiefungen von zur Nutzlast gehörenden Schrauben pipettiert (Abb.1e). Für das Auftragen der Proben 13–15 auf der Unterseite der Nutzlast wurden die ausgewählten Bereiche markiert, gesäubert und die DNA aufgetragen (Abb.1f.). Bild: PLOS ONE
Ins Weltall und zurück TEXUS-49 konnte neun Tage nach dem Aufbringen der DNA starten (Abb.2). Nach Ausbrennen und Separation der zweistufigen Raketenmotoren erreichte die Nutzlast während des rund 13-minütigen ballistischen Fluges eine Höhe von 268km und eine 378s dauernde Schwerelosigkeitsphase. Die Flugbahn wurde mittels GPS verfolgt und die Nutzlast nach Landung per Helikopter geborgen. Die Wiedereintrittsgeschwindigkeit in die Erdatmosphäre lag bei 1–2km/s, wobei Temperaturen zwischen 118 und 130°C (Innenseite der Nutzlast) und 1.000°C (geschätzte Temperatur der umgebenden Gase) auftraten.
Abb.2 Start der TEXUS-49 Höhenforschungsrakete am 29.03.2011 um 6:01 Uhr Bild: Adrian Mettauer
Die Überraschung Anschließend wurde die Plasmid-DNA durch Auftragen eines angewärmten Tris-Puffers wieder in Lösung genommen (Abb.?3) und bis zum Zeitpunkt des Rücktransportes bei -20°C gelagert. Zuerst wurde die Konzentration und Reinheit der DNA photometrisch bestimmt und die Wiedergewinnungsrate berechnet. Dann die Überraschung: An allen Auftragsstellen wurde Plasmid-DNA wiedergefunden, an einer Stelle sogar 53% der aufgetragenen Menge. Mit diesem Ergebnis haben wir niemals gerechnet, wir hätten maximal geringe Spuren von zerstörten DNA-Resten erwartet. Ein Teil der Proben wurde dann auf ein Agarosegel geladen und der Grad der Degradation nach erfolgter Elektrophorese bestimmt.
Abb.3 Wiedergewinnung der DNA. Nach erfolgreichem Flug und Rücktransport zum Esrange Space Center wurde die Nutzlast weitestgehend von Schnee und Eis befreit und die markierten Stellen, an denen vor dem Flug die Test-DNA aufgetragen worden war, wurden mit vorgewärmter Pufferlösung benetzt, um die getrocknete DNA wieder in Lösung zu bringen. Bild: Adrian Mettauer
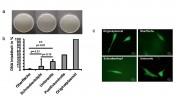
DNA überträgt weiterhin genetische Information Die Integrität der Plasmid DNA wurde mittels Transformation in Escherichia coli und nachfolgender Antibiotika-Selektion mit Kanamycin analysiert (Abb.4ab). Die Abbildung zeigt, dass sehr viele Plasmid-DNA Moleküle noch intakt gewesen sein mussten, da nur diese eine Antibiotikaresistenz in Bakterien vermitteln. Weiterhin wurde die Plasmid-DNA ebenfalls in eukaryotische Fibroblasten-Zellen eingebracht und die Expression des GFP mittels Fluoreszenzmikroskopie verfolgt (Abb.4c). Bei allen für die Transfektion ausgewählten Proben konnten eindeutig fluoreszierende Zellen identifiziert werden. Dies ist der zweite unabhängige Beweis, dass ein Teil der eingesetzten DNA den Flug auf der Außenseite der Nutzlast ins Weltall und zurück überstanden hat und als Träger der genetischen Information intakt geblieben ist.
Abb.4 DNA überträgt nach Raumflug und Wiedereintritt weiterhin genetische Informationen. Die nach Raumflug und Wiedereintritt wiedergewonnene Plasmid-DNA wurde in Escherichia coli KRX transformiert (Abb.4a) und die Intaktheit wurde, basierend auf der Transformationseffizienz in Kolonien, pro Nanogramm DNA berechnet (Abb.4b). Signifikant höhere Resultate wurden bei den Proben, die auf der Nutzlastunterseite aufgetragen wurden, erhalten (p-Wert: 0,01 für den Vergleich Oberfläche versus Unterseite) (Anzahl der Proben: Oberfläche n=4, Schraubenköpfe n=8, Unterseite n=3, Positivkontrolle n=1, original Plasmid DNA n=1) (p-Werte sind für paarweise Analysen angegeben) (Quelle: PLOS ONE). Für jede Testposition (Oberfläche, Schraubenköpfe, Unterseite) wurde eine repräsentative Probe ausgewählt und die DNA in NIH-3T3-Mausfibroblasten transfiziert. Die Expression des grün fluoreszierenden Proteins (GFP) wurde nach einem Tag Inkubationszeit analysiert. In allen Proben konnte GFP-Expression fluoreszenzmikroskopisch nachgewiesen werden, was auf vollständig funktionale Plasmid-DNA hinweist (Abb.4c). Die DNA konnte nach Raumflug und Wiedereintritt in die Erdatmosphäre genetische Information korrekt weitergeben.
Was macht die DNA weltraumtauglich? Wir vermuten, dass die Test-DNA durch den Salzgehalt der Probe und die extreme Trockenheit im Vakuum des Weltalls so gut stabilisiert worden ist, dass sie den heißen Wiedereintritt in die Erdatmosphäre überstand. Studien am Boden haben kürzlich gezeigt, dass gefriergetrocknete Plasmid-DNA extrem stabil ist und enorme Überlebenszeiten hat [6]. Die bei unserem Experiment herrschenden Bedingungen waren möglicherweise besonders günstig für das Überleben der DNA. Zukünftige Studien werden die einzelnen Bedingungen in Relation zueinander analysieren und versuchen, den oder die entscheidenden Faktoren zu identifizieren, die letztlich dann für Vorhersagemodelle des postulierten Transfers von DNA zwischen Himmelkörpern dienen könnten. Ist die Erde wirklich biologisch isoliert? Auch wenn die zugrunde liegenden Faktoren letztlich noch identifiziert werden müssen, zeigt das Experiment, dass DNA grundsätzlich in der Lage ist, den Eintritt in die Erdatmosphäre aus dem Weltall zu überstehen. Und zwar nicht auf der Basis einer Annahme oder eines Modells, sondern aufgrund eines realen Experimentes. Das bedeutet, dass wir grundsätzlich annehmen müssen: Sollte DNA außerhalb unseres Planeten existieren und in kosmischem Staub oder in Meteoriten zur Erde gelangen, könnte sie auch den Eintritt in die Erdatmosphäre überstehen. Wir müssen damit rechnen, dass unsere Erde auch beim Transfer von Bausteinen des Lebens und genetischer Information keinesfalls von kosmischen Ereignissen und Vorgängen isoliert ist. Auch wenn die zeitlichen und räumlichen Dimensionen uns an und über die Grenzen unserer Vorstellungskraft führen. Aber das ist nur ein Problem unseres Vorstellungsvermögens.
Literatur Dem Artikel liegt folgende Originalarbeit zugrunde: Cora S. Thiel, Svantje Tauber, Andreas Schütte, Burkhard Schmitz, Harald Nuesse, Ralf Möller, Oliver Ullrich. Functional Activity of Plasmid DNA after Entry into the Atmosphere of Earth Investigated by a New Biomarker Stability Assay for Ballistic Spaceflight Experiments. PLOS ONE. November 26, 2014. DOI:10.1371/journal.pone.0112979 Bild: © istockphoto.com|adventtr |
L&M 3 / 2015
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Die Autoren:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |