|
Bio&Biotech
 >
Euphorbia pulcherrima und andere
>
Euphorbia pulcherrima und andere
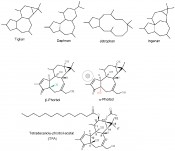
Euphorbia pulcherrima und andereDer Weihnachtsstern, der nach dem Botaniker J. R. Poinsette auch Poinsettie genannt wird, zählt zu den weltweit beliebtesten Zimmerpflanzen. Nur in der Adventszeit kann man ihn kaufen, denn der Kältereiz in dieser Jahreszeit sorgt dafür, dass sich in den Anbaubetrieben die intensiv rote Farbe der Hochblätter und der kompakte Wuchs optimal entwickeln. Die Wildform dieser ursprünglich aus Mexiko stammenden, zu den Euphorbiaceae zählende Pflanze kann bis zu 2 m hoch werden mit bis zu 15 cm langen, gezähnten Blättern. Sie enthalten in ihrem Milchsaft die hautirritierenden Diterpenester des 13-Hydroxyingenols. Von der kultivierten Zimmerpflanze ist bekannt, dass sie keine bzw. nur in Spuren Giftstoffe enthält. Euphorbia ist die artenreichste Gattung der Wolfsmilchgewächse, der „Wolf“ im Namen soll darauf hinweisen, dass der milchige Saft meistens giftig ist. Neben den toxischen und zum Teil äußerst hautirritierenden Eigenschaften wird oft ein interessantes pharmakologisches Potenzial beobachtet. Einige Vertreter sind außerdem wichtige Wirtschaftspflanzen. Phorbolester – hautirritierend Die erste, rein isolierte Verbindung aus Euphorbiaceae war das Phorbol. Es wurde bereits 1934 aus den Samen des Crotonölbaumes (Croton tiglium) gewonnen. Die Struktur wurde aber erst 1967 durch die Forschungsgruppe von E. Hecker (DKFZ Heidelberg) aufgeklärt [1]. Hunderte von Diterpenen wurden in den letzten Jahrzehnten aus Euphorbiaceae isoliert [2], darunter z.B. die Diterpenklassen der Tigliane, Daphnane, Ingenane und Jatrophane (Abb. 1). Ihr Oxidationszustand schwankt erheblich, OH-Gruppen sind oft mit Carbonsäuren verestert. Doppelbindungen treten sowohl endo- als auch exozyklisch in fast allen Positionen auf. Bei allen Verbindungen ist der Cyclopentanring mit dem Rest des Moleküls trans verknüpft, die absoluten Konfigurationen an C-3, C-4 und C15 sind identisch. Der Name Phorbol steht für eine Reihe oxidierter und hydroxylierter Tigliane mit verschiedenen Estergruppen. Die Position der OH-Gruppe an C-4 bestimmt dabei, ob eine Substanz irritierend ist (β-Form) oder nicht (α-Form). In der α-Form verhindert die räumliche Anordnung von OH-4 zu Ring D, dass PKC (Protein-Kinase C) und andere Phorbolester-Rezeptoren aktiviert werden. Auch geringe Änderungen in der Struktur wie die Umsetzung von ß-4-OH zu ß-4-OCH3 verringern die irritierende Wirkung. Ähnlich wirkt die Einführung unterschiedlicher Estergruppen an C-12, sie führt lediglich zu einer Variation in der Wirkstärke. Tetradecanoyl-phorbol-acetat (TPA), der wichtigste Vertreter dieser Gruppe, besitzt das Grundgerüst eines Tiglian-Diterpens (Abb. 1). TPA ist der stärkste bekannte Tumorpromotor und wird dazu verwendet, molekulare Mechanismen in der Krebsforschung, Immunologie und Toxikologie zu untersuchen. Über 22 000 Publikationen sind in den letzten 40 Jahren darüber erschienen [3]. Bei Tumorpromotoren handelt es sich um Substanzen, die für sich im Tierversuch keine Hauttumoren erzeugen, jedoch in der zuvor mit einer sub-karzinogenen Dosis eines Karzinogens behandelten Haut stufenweise zu multiplen benignen und malignen Tumoren führen. Erstaunlicherweise führt die Einführung einer Methylgruppe an C-4 neben der verringerten Entzündlichkeit auch zum Verlust der tumorpromovierenden Aktivität. Intensiv untersucht wurde der Einfluss von TPA auf die Proteinkinase C, die eine bedeutende Rolle bei der Signalübertragung, dem Zellwachstum, der Zelldifferenzierung und beim programmierten Zelltod (Apoptose) spielt. Die Toxizität von Phorbolestern hängt wie bei vielen anderen Substanzen auch von der Dosis und der Dauer der Exposition ab. Höhere Konzentrationen erhöhen die Toxizität, eine Überdosis ist für Mikroorganismen und höhere Lebewesen bei oraler Verabreichung letal. Phorbolester lassen sich in nicht toxische Substanzen überführen und können dann pharmakologisch interessante Eigenschaften zeigen.
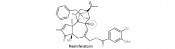
Abb.1 Beispiele einiger Diterpenklassen aus Euphorbiacae; Strukturen von α- und β-Phorbol und des Tetradecanoyl-phorbol-acetats (TPA). Resiniferatoxin – schärfer als Capsaicin und schmerzlindernd In Marokko wächst eine Wolfsmilchpflanze (E. resinifera) von kaktusähnlichem Aussehen. Sie enthält als wirksame Substanz das Resiniferatoxin (RTX). Dieselbe Substanz findet man auch in der in Nordalgerien vorkommenden E. poissonii. RTX (Abb. 2) ist auf der so genannten Scoville-Skala tausendmal schärfer als Capsaicin, was etwa 16 Mio. Scoville-Einheiten entspricht. Beide Substanzen verursachen ein stark brennendes Gefühl an jeder Körperstelle, mit der sie in Kontakt kommen [4]. RTX wirkt auf die Plasmamembran sensorischer Neuronen und macht sie durchlässig für Kationen, insbesondere Calcium. Zunächst wirkt es stark reizend, dann aber stark schmerzdämpfend. Obwohl beide Substanzen Capsaicin und Resiniferatoxin anfangs als schmerzhaft heiß empfunden werden, können sie zur Schmerztherapie eingesetzt werden. RTX zeigt aber noch eine weitere interessante Eigenschaft. Eine Injektion in die Rückenmarksflüssigkeit zerstört offenbar die das Protein TRPV1 (transient receptor potential vanilloid 1) produzierenden Nervenzellen, die verantwortlich sind für die Übertragung des Entzündungsreizes. Dabei sind andere Schmerzempfindungen nicht betroffen, etwa Schmerz durch einen Nadelstich oder Zwicken. RTX könnte also helfen, durch Entzündungen auftretende Schmerzen dauerhaft zu lindern.
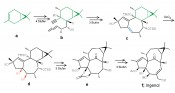
Abb.2 Struktur von Resiniferatoxin. Ingenol gegen aktinische Keratose Verschiedene Euphorbiaceae wie E. peplus, E. palustris oder E. lathyris enthalten als Wirksubstanzen Ingenolester, die in der traditionellen Medizin zur Behandlung von Tumoren, Migräne, Parasiten oder gar als Abführmittel verwendet wurden. Höhere Dosen erweisen sich als toxisch und teilweise auch letal. Der Kreuzwolfsmilch (E. lathyris) wird nachgesagt, die Pflanze halte im engeren Umkreis von etwa 3 – 4 m Wühlmäuse und Maulwürfe fern. Ingenol und Ingenolester enthalten als Basisstruktur das Ingenan (Abb. 1). Ingenol wurde erstmals 1968 von der Arbeitsgruppe um E. Hecker aus E. ingens isoliert [5]. In den Blickpunkt geriet kürzlich das Ingenolmebutat, ein Angelicasäurederivat, nachdem seine Wirkung gegen die aktinische oder solare Keratose (eine fakultative Präkanzerose) bekannt wurde. In kontrollierten Studien bildeten sich nach sechs Wochen über 40 der Keratosen komplett zurück. Die Gewinnung von Ingenol z.B. aus E. peplus als Bezugsquelle ist unwirtschaftlich, denn aus 1kg Pflanzenmaterial können lediglich etwa 1,1mg gewonnen werden. L. Jørgensen et al. haben nun einen synthetischen Zugang gefunden [6]. In 14 Stufen, ausgehend von (+)-Caren, wird zunächst in Cyclaseschritten und danach in Oxidaseschritten das Molekül aufgebaut (Abb. 3). Die Ausbeuten sind deutlich höher als bei den bisher publizierten Total- und Semisynthesen.
Abb.3 Die Synthese von Ingenol (f), ausgehend von (+)-Caren (a): Die Cyclisierungsreaktion über b zu c erfordert sieben Reaktionsschritte, die sich anschließenden Oxidationsschritte umfassen ebenfalls sieben Reaktionsstufen und führen über d und e zum Zielmolekül.
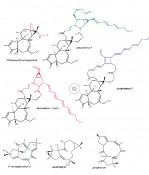
Abb.4 Sechs Phorbolester sind im Jatrophaöl enthalten. Abgebildet sind Jatrophafakor 1, 3, 4 und 5. Sie enthalten das 12-Desoxy-16-hydroxyphorbol als Grundgerüst. Die drei Diterpene 2-Hydroxyjatrophan, Japodagrin und Jatropatrion enthalten das Jatrophan als Grundgerüst. Biodiesel aus Jatropha Curcas Jatropha curcas ist auch unter dem Namen Purgiernuss bekannt, weil sie früher als Abführmittel benutzt wurde. Die Pflanze ist äußerst robust, verträgt lange Trockenperioden und wächst auch auf ertragsschwachen Böden. Selbst in trockenen Savannengebieten, z.B. in Tansania, gedeiht die Pflanze. Sie ist damit ideal geeignet für die Wiederaufforstung von Flächen, die wegen Dürre oder Bodenerosion aufgegeben wurden. Weltweit liegt die Anbaufläche derzeit noch bei < 1 Mio. Hektar, wovon der Großteil vor allem auf Indien, China und Indonesien entfällt. Trotz der geringen Ansprüche an Boden und Klima enthalten die Samen etwa 33% Öl mit der beachtlichen Cetanzahl von 60 (Raps: 54). Die Verarbeitung des Öls zu Biodiesel liefert unter optimalen Anbaubedingungen bis zu 2.200l pro Hektar. Der kommerzielle Anbau von Jatropha curcas ist deshalb besonders lohnend. Kaltgepresstes Öl kann in angepassten Motoren direkt verwendet werden und erspart damit finanzschwachen tropischen Ländern den Import teuren Erdöls. Sowohl das kaltgepresste Öl (etwa 3,4mg/g) als auch der Presskuchen enthalten toxische Phorbolester. Während des Produktionsprozesses von Biodiesel werden die Phorbolester vollständig abgebaut, im proteinreichen Presskuchen verbleiben sie aber, er ist deshalb nicht ohne weitere Bearbeitung als Viehfutter verwertbar. Bisher wurden sechs Phorbolester isoliert. Grundgerüst ist das 12-Desoxy-16-hydroxyporbol, das mit seltenen, exotisch anmutenden Dicarbonsäuren über OH-13 und OH-16 verestert ist (Abb. 4). Die Phorbolester im Jatrophaöl zeigen die typischen cytotoxischen Effekte, wirken aber auch insektizid und antimikrobiell und sollen z.B. als Abwehrmittel gegen den Schädling Spodoptera frugiperda wirken. Jatrophapflanzen enthalten in allen Pflanzenteilen eine Vielzahl terpenioder Substanzen. Über 60 Diterpene wurden bisher beschrieben [2, 7], die wegen ihrer neuartigen Strukturen und ihrer potenziellen medizinischen und pharmakologischen Verwendung Interesse gefunden haben. Sie zeigen in vitro cytotoxische (z.B. 2-Hydroxyjatrophon, siehe Abb.4), antibakterielle (z.B. Japodagrin), fungizide oder Antitumorwirkungen (z.B. Jatrophatrion).
Literatur Herrn Dr. Jürgen Schweizer, DKFZ Heidelberg, sei gedankt für wertvolle Hinweise zu den Phorbolestern als Tumorpromotoren. Foto: © panthermedia | teena13 |
L&M 8 / 2013
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |