|
Chemie
 >
Neopterinscreening als Schutzwall vor Virusinfektionen
>
Neopterinscreening als Schutzwall vor Virusinfektionen
Neopterinscreening als Schutzwall vor VirusinfektionenNeue Erreger ante portas!Insbesondere durch die zurzeit in Westafrika grassierende Ebola-Epidemie stehen Viruserkrankungen momentan im Fokus der Öffentlichkeit und Infektionswege werden ebenso diskutiert wie Infektionsprophylaxe. Ein besonderer Aspekt der Infektionsprophylaxe – wenn auch weniger im Zusammenhang mit dem Ebolavirus – ist die Vermeidung von Virusübertragungen bei Bluttransfusionen. Man mag sich vielleicht noch an auf diese Weise übertragene AIDS-Erkrankungen erinnern, aber es gibt noch eine ganze Reihe weiterer Viren mit nicht unerheblichem Risikopotenzial hinsichtlich Bluttransfusion, sodass die Entwicklung möglichst universeller Screeningverfahren von großer Bedeutung ist.
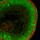
Abb.1 Neopterin ist ein Signalbotenstoff, der während der zellulären Immunreaktion verstärkt gebildet wird. Drastisch erhöhte Neopterinspiegel werden vor allem bei akuten Virusinfektionen beobachtet.
33 Jahre AIDS und AIDS-Forschung 1981 wurde mit AIDS eine total neue, durch Blut und Sexualkontakte übertragbare Erkrankung bekannt. AIDS ist besonders heimtückisch. Oft erst Jahre nach der Ansteckung mit dem humanen Immundefizienzvirus (HIV) beginnt die Immunfunktion zu versagen und damit bricht die voll ausgeprägte Erkrankung aus. Nach mehr als 30 langen Jahren intensivster Forschung in den bedeutendsten Zentren der Welt stehen nun gut wirksame und verträgliche Medikamente zur Verfügung. Sie unterbinden zumeist die Vermehrung des HIV – allerdings vorerst nur bei Patienten in den reicheren westlichen Ländern der Erde. Bis heute ist es nicht gelungen, durch eine prophylaktische Impfung die weitere Verbreitung des Virus einzudämmen oder gar zu verhindern. Und es ist weiterhin fraglich, ob es jemals gelingen kann, bei infizierten Patienten das HI-Virus vollständig zu eliminieren. Bei den Betroffenen bleibt HIV also weiterhin im Körper nachweisbar, wenn auch – unter adäquater Therapie – nur in geringer Konzentration. Trotzdem bleiben Körperflüssigkeiten dieser Menschen infektiös, wenn auch nur geringfügig. Sie sind potenziell immer noch in der Lage, HIV an andere Personen zu übertragen.
Neue Herausforderung für das Blutspendewesen AIDS war aber nicht nur eine Herausforderung für die medizinische Forschung. Eine neue Strategie für hohe Virussicherheit bei der Bluttransfusion zu musste her. Durch ein zusätzliches Screening auf Anti-HIV-Antikörper konnte das Problem verkleinert werden – ja, schon bis auf die „diagnostische Fensterperiode“. Das ist die Zeit, in der Betroffene zwar infiziert sind, aber noch keine Antikörper gebildet haben. Tatsächlich gibt es ein generelles Problem im Blutspendewesen: Das Spendenscreening basiert (entsprechend einer WHO-Richtlinie) exklusiv auf erregerspezifischen Tests. Der Einsatz solcher Tests setzt aber voraus, dass man den Krankheitserreger bereits erkannt hat, ihn charakterisieren konnte und dass man einen entsprechenden Screeningtest zur Verfügung hat. Der Bluttrans- fusionsempfänger ist ohne solche Tests relativ ungeschützt. Im Fall von HIV retrospektiv betrachtet: Es hat etliche Jahre vom ersten Auftreten des Virus in der westlichen Welt bis zum Einsatz des Antikörperscreenings im Jahr 1985 gedauert. Allerdings wurden einige zusätzliche vorbeugende Maßnahmen ergriffen, um das Risiko zu vermindern. So wurden z.B. bestimmte Spendergruppen mit hohem Infektionsrisiko von der der Blutspende generell ausgeschlossen.
Hepatitis-C-Prophylaxe Ähnlich wie bei HIV wurde das spezifische Antikörperscreening auf das Hepatitis-C-Virus erst mehr als 20 (!) Jahre nach der Erkenntnis eingeführt, dass es neben dem Hepatitis-A- und Hepatitis-B-Virus auch noch einen weiteren viralen Erreger geben muss, der durch Bluttransfusion übertragbar ist und eine oftmals tödliche Lebererkrankung verursachen kann. In der Zwischenzeit haben Blutspendedienste zur Risikominderung sogenannte Leberfunktionsproben als Surrogatteste verwendet. In Österreich gab es dabei große Unterschiede in der Reaktionszeit zwischen den verschiedenen Bundesländern: Während die Blutbank der Universitätsklinik in Innsbruck bereits Mitte der 80er-Jahre entsprechend reagiert hatte, gab es andere Bundesländer mit mehr als 15–20 Jahren Verzögerung. Nach einer Pilotstudie im Jahr 1985 setzte das österreichische Bundesland Tirol seit 1986 auf eine zusätzliche Strategie: Neben den üblichen Testverfahren wird seither jede Blutspende zusätzlich auf den Neopteringehalt untersucht. Neopterinscreening zur Risikominderung in Österreich Neopterin ist ein Stoff, der während der sogenannten zellulären Immunantwort von Zellen des menschlichen Immunsystems vermehrt gebildet wird (Abb.1). Ein Neopterintest ist nicht spezifisch für virale Erreger, spricht aber bei Infektionen mit allen Viren sehr rasch an. Die Konzentrationen im Blut steigen noch lange vor der Bildung der spezifischen Antikörper an, nach denen im üblichen Screening gesucht werden. Die Ergebnisse von 76.578 Blutspenden wurden in der Deutschen Medizinischen Wochenschrift veröffentlicht [1]. Mit einem Neopteringehalt von 10nmol/L wurde ein sinnvoller Grenzwert definiert, mit dem circa 1,7% der Blutspenden von der Transfusion ausgeschlossen werden mussten. Es wurde in verschiedenen Nachfolgestudien nachgewiesen, dass diese Strategie in der Lage ist, das Übertragungsrisiko für verschiedene weitverbreitete virale Erreger wie Zytomegalievirus (CMV), Epstein-Barr-Virus, Parvovirus B19 und auch Hepatitis-C-Virus signifikant zu verringern. Ein entscheidender strategischer Vorteil des Neopterintests ist aber, dass man auch neu auftretende virale Erreger detektieren kann, selbst wenn ein Risiko überhaupt noch nicht erkennbar ist. Auch bei Viren, die zu selten sind, als dass sich aufgrund einer einfachen Kosten-Nutzen-Abschätzung ein spezifisches Screening rechtfertigen ließe, kann eine signifikante Risikominderung erreicht werden. Aufgrund der positiven Erfahrungen mit dem Neopterinscreening in Tirol wurde es Mitte der 1990er-Jahre auf ganz Österreich ausgedehnt. Neopterinscreening – eine Strategie für den asiatischen Raum … Derzeit wird in Zusammenarbeit unserer beiden Forschungsteams in Innsbruck und an der HKUST in Hongkong geprüft, ob die Neopterinuntersuchung die Virussicherheit im Blutspendewesen auch im ostasiatischen Raum verbessern kann. Gerade in Asien war man in der vergangenen Dekade schon mehrfach vom Auftreten neuer Epidemien – z.B. dem durch ein Coronavirus ausgelösten schweren akuten Atemwegssyndrom (SARS) und der durch Influenza-A Virus H5N1 verursachten Vogelgrippe – betroffen. Dazu kommt noch das Risiko, das dem in in Ostasien weitverbreiteten und durch verschiedene Stechmücken übertragenen Denguevirus ausgeht. Patienten, die wegen dieser Infektionskrankheiten hospitalisiert wurden, zeigten allesamt erhöhte Neopterinspiegel. Natürlich wurden diese Patienten aufgrund einer ausgeprägten Symptomatik eingeliefert und wären als für die Blutspende ungeeignet erkannt worden. Aber man kann davon ausgehen, dass die Neopterinspiegel schon vor dem Erstuntersuchungszeitpunkt bzw. vor dem Auftreten signifikanter Infektionssymptome erhöht war. Als Konsequenz ist derzeit ein neuartiges Testverfahren in Entwicklung, weil es in China vorgeschrieben ist, Tests für die Infektionssicherheit einer Spende schon vor der Blutabnahme durchzuführen. …?und für die aktuelle Ebola-Epidemie Mit Ebola geriet ein schon seit längerer Zeit bekanntes Virus erneut in den Fokus. Die gegenwärtige Epidemie in den westafrikanischen Ländern Guinea, Liberia und Sierra Leone zeigt, dass es immer wieder zum Aufflackern solcher Epidemien kommen kann und dass wegen der verbesserten Verkehrsanbindung auch eine Verbreitung außerhalb der betroffenen Staaten zwar selten, aber doch möglich ist. So wurde am 29. September 2014 erstmals ein Fall von Ebola-Fieber in den USA in einem Hospital in Dallas, Texas nachgewiesen. Der Patient hatte sich in Liberia infiziert. Auch wenn die Luft in Flugzeugen mit kurzen Intervallen ausgetauscht wird, ist unklar, inwieweit es ein Ansteckungsrisiko für Mitreisende gibt. Ebenso ist unklar, wie hoch das Ansteckungsrisiko für Personen aus seinem näheren Umfeld war. Bei mit dem Ebolavirus infizierten Patienten wurden durch französische Wissenschaftler bereits 2002 erhöhte Neopterinspiegel im Blut nachgewiesen, und der Grad der Erhöhung gab eine Indikation für die zu erwartende Überlebenszeit der Patienten [2].
Daraus ergibt sich zumindest ein Hinweis darauf, dass eine Ansteckung mit dem Ebolavirus zu einem Ansteigen der Neopterinkonzentration im Blut und auch im Urin führt. Das wiederum eröffnet die Möglichkeit, Personen im Umfeld einer infizierten/erkrankten Person auf potenzielle Infektion testen zu können.
Abb.2 Mittelwerte von CRP, Neopterin & C/N Ratio bei bakteriellen und viralen Infektionen
Das Auftreten der Ebola-Epidemie in Westafrika bestätigt erneut, dass es jederzeit zum Aufflackern eines viralen Erregers kommen kann. Das kann, wie im Fall von Ebola, zu einer Bedrohung vor allem der näheren Umgebung führen. Durch die kurze Inkubationszeit mit ausgeprägter Symptomatik kann einer weiträumigeren Ausbereitung durch geeignete seuchenpolitische Maßnahmen entgegengewirkt werden. Wesentlich schwieriger gestaltet sich die Situation jedoch im Fall von klinisch unauffälligerem Krankheitsgeschehen. So wissen beispielsweise HIV-Infizierte häufig selbst dann noch nichts über ihren Infektionsstatus, wenn sich eine zunehmende Immunschwäche bereits abzeichnet. Neue Viren stehen vor den Toren! MIt dem Neopterinscreening können ein prophylaktischer Schutzwall errichtet und ein „gestrenger Torwächter“ etabliert werden.
Literatur |
L&M 9 / 2014
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Die Autoren:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |