|
APOE4 als wichtigster Risikofaktor der Alzheimererkrankung
APOE4 als wichtigster Risikofaktor der AlzheimererkrankungBaustein im DemenzpuzzleDas APOE-Gen liegt in drei polymorphen Allelen vor, dem APOE2-, 3- und 4- Genotyp. Der APOE4-Genotyp ist der wichtigste genetische Risikofaktor für die Alzheimererkrankung. Die Expression der Genotypen APOE2, 3 und 4 führt zu den untereinander leicht unterschiedlichen Proteinen (i.e. Isoformen) ApoE2, 3 und 4. Diese kleinen Unterschiede in Aufbau und Struktur dieser drei Proteine haben wichtige Auswirkungen auf verschiedenste Prozesse im Gehirn und führen bei APOE4-Genträgern zu einem relevant erhöhten Risiko, an Alzheimer zu erkranken. Die bestbekannten ursächlichen Mechanismen sind dabei der lokale Abbau sowie der Abtransport von Amyloid-beta, die ApoE-Rezeptoren-vermittelten Prozesse, welche synaptische Plastizität, Tau-Phosphorylierung und Neuroprotektion beeinflussen, der zentrale Lipidmetabolismus sowie die Neuroinflammation. Der periphere Lipidmetabolismus (daher ist das Protein den meisten bekannt; es ist z.B. mit Auftreten von Hyperlipidämie, Arteriosklerose und koronarer Herzkrankheit assoziiert) spielt bei der Entstehung und Progression der Alzheimererkrankung vermutlich eine untergeordnete Rolle.
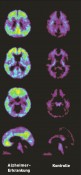
Abb.1 Positronen-Emissions-Tomografie des Gehirns in verschiedenen axialen Ebenen (obere drei Bilder) und einer sagittalen Darstellung (unterste Bilderreihe) mit Pittsburgh Compound B bei einer Person mit Alzheimererkrankung (links) und einer gesunden Kontrolle. Der Tracer weist fibrilläre Amyloid-beta-Ablagerungen im Gehirn nach. Die Ablagerungen stellen sich grün-gelblich dar. Diese Ablagerungen werden eng mit dem Auftreten einer Alzheimererkrankung in Verbindung gebracht. ApoE4 hat einen Einfluss auf die Ausbildung dieser Amyloid-beta-Ablagerungen: Sie treten bei APOE4-Trägern mit höherer Wahrscheinlichkeit als bei Nicht-APOE4-Trägern auf. Wenn sie bei APOE4-Trägern auftreten, dann in größerer Menge und früher im Verlauf des Lebens als bei Nicht-APOE4 Trägern. Auch ist bei Vorliegen der Ablagerungen das Risiko bei APOE4-Trägern gegenüber Nicht-APOE4-Trägern erhöht, zukünftig an einer Alzheimerdemenz zu erkranken. Wichtigster genetischer Risikofaktor Genomweite Assoziationsstudien haben bestätigt, was viele Wissenschaftler schon länger vermutet haben: Der APOE4-Genotyp ist der wichtigste genetische Risikofaktor für die Alzheimererkrankung. Das APOE-Gen existiert in drei Genotypen. Die Prävalenz des APOE2-Genotyps weltweit beträgt etwa 8%, des APOE3-Genotyps etwa 78% und des APOE4-Genotyps etwa 14%. Folgende Zahlen fassen das relevant erhöhte Risiko für APOE4-Genträger wohl am anschaulichsten zusammen: Wenn eine Person Träger von zwei APOE4-Allelen (also APOE4-homozygot) ist, hat sie eine 90%ige Wahrscheinlichkeit, mit 68 Jahren an einer Alzheimererkrankung zu leiden. Wenn sie ein APOE4-Allel hat (also APOE4-heterozygot ist), dann besteht eine Wahrscheinlichkeit von 47%, mit 76 an der Krankheit zu leiden. Wenn kein APOE4-Allel vorliegt, besteht eine Wahrscheinlichkeit von 20%, mit 84 Jahren zu erkranken (siehe auch [4]). ApoE spielt in viele Mechanismen der neuralen und neuronalen Homöostase hinein, die folgenden Mechanismen werden jedoch für diese deletären Zusammenhänge in diesem Zusammenhang hauptverantwortlich gemacht: Amyloid-beta-assoziierte Mechanismen Amyloid-beta spielt eine zentrale Rolle bei der Alzheimererkrankung. Die Ablagerung von Amyloid-beta enthaltenden Plaques im Hirngewebe sowie in Gefäßen von Alzheimerpatienten stellt das pathologische Pendant dazu dar. Die Ablagerungen können autoptisch nachgewiesen werden, aber auch in vivo mittels Positronen-Emissions-Tomografie (Abb.1) und, mit vergleichbarer Sicherheit, im Nervenwasser. Es wird heute angenommen, dass bei der häufigsten Form der Alzheimererkrankung, der späten Form (die frühe Form ist sehr selten), defekte Aufräum-(i.e. Clearance-)Mechanismen die Ablagerungen dieses Amyloid-beta-Peptids verursachen. In diese Clearance-Mechanismen sind die ApoE-Proteine isoform-spezifisch (also unterschiedlich, je nachdem, ob ein ApoE2-, 3- oder 4-Protein vorliegt) involviert, die ApoE4-Isoform hat dabei die ungünstigsten Eigenschaften. Folgende Zahlen aus einer großen populationsbasierten Kohorte reflektieren diesen drastischen Einfluss der ApoE4-Isoform: Während sich bei 41% der 50–59 jährigen APOE4-Träger fibrilläre Plaques im Gehirn nachweisen lassen, sind es nur 8% der Gleichaltrigen ohne ein APOE4-Allel [3]. Diese frühe Manifestation der Amyloid-beta-Ablagerungen spiegelt ein wichtiges Phänomen der Alzheimererkrankung wider: Die Bildung dieser pathologischen Ablagerungen geht den klinischen Symptomen Jahre, wenn nicht Jahrzehnte voraus. Das Vorliegen des APOE4-Allels ist aber nicht nur mit einer erhöhten Wahrscheinlichkeit verbunden, dass die Personen Amyloid-beta-Ablagerungen im Gehirn bekommen, sondern auch mit einem deutlich erhöhten Risiko, später an der Alzheimerdemenz tatsächlich zu erkranken. Personen mit einem milden kognitiven Defizit (mild cognitive impairment, MCI; dabei handelt es sich um ein in der älteren Bevölkerung häufig anzutreffendes Symptom mit leichten Einschränkungen der kognitiven Leistungen) und zumindest einem APOE4-Allel haben ein höheres Risiko, eine Alzheimerdemenz zu bekommen als Personen mit APOE2- und 3-Allelen [8]. Es drängt sich an der Stelle natürlich die Frage auf, warum es evolutiv überhaupt Sinn macht, ein (oder gar zwei) APOE4-Allel(e) zu besitzen. Dies dürfte am ehesten an einem Vorteil liegen, den Personen mit diesen Genotypen in der frühen ontogenetischen Entwicklung gegenüber Nicht-APOE4-Trägern haben: APOE4-positive Kinder und junge Erwachsene weisen im Durchschnitt bessere kognitive Leistungen als Gleichaltrige ohne diesen Genotyp auf [7]. Erst das Erreichen von Überlebenszeiten über das 5. Lebensjahrzehnt hinaus im Verlauf der letzten Jahrhunderte der Menschheitsentwicklung haben die Nachteile dieses Genotyps sichtbar werden lassen. Auch bei der Parkinson-Demenz scheint die Amyloid-beta-Pathologie eine Rolle zu spielen: In einer aktuellen Studie in Zusammenarbeit mit dem Karolinska-Institut in Stockholm konnten wir nicht nur den Zusammenhang von Amyloid-beta-Pathologie und Demenz bei Parkinson bestätigen, sondern auch zeigen, dass dies mit einer erhöhten Wahrscheinlichkeit einhergeht, Träger von APOE4 zu sein und hohe Werte des ApoE Proteins im Nervenwasser aufzuweisen [9]. Wie sind nun diese unterschiedlichen Wahrscheinlichkeiten des Auftretens von Amyloid-beta-Pathologie und nachfolgender Alzheimerdemenz mit APOE-Genotyp und ApoE-Isoformen in Verbindung zu bringen? Wie bereits erwähnt, spielen besonders die ApoE4-assoziierten Defizite von Amyloid-beta-Clearance eine wichtige Rolle. So transportiert das ApoE4-Protein Amyloid-beta langsamer aus dem Gehirn als die beiden anderen Isoformen und ApoE-bindende Rezeptoren reagieren oft weniger effizient auf die ApoE4-Isoform. Beispiele für derartige Rezeptoren sind der ApoE-Rezeptor 2 und der Low density lipoprotein receptor-related protein 1 (LRP1)-Rezeptor. Der ApoE-Rezeptor 2 ist gekoppelt an NMDA-Rezeptoren (wichtig für Synapsenfunktion, Lernen und Merkfähigkeit). Der LRP1-Rezeptor kann über die GSK3beta-Aktivität die Phosphorylierung von Tau beeinflussen. Eine Hyperphosphorylierung von Tau, ein charakteristisches Merkmal von an Alzheimer erkrankten Gehirnen, führt zu einer Einschränkung des Axontransports und damit zu einer Einschränkung der Kommunikation zwischen den Synapsen und dem Zellkern.
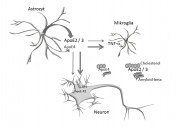
Abb. 2 Als hauptrelevant für die Entstehung und Progression der Alzheimer-erkrankung eingeschätzte Mechanismen, in die ApoE involviert ist. ApoE wird hauptsächlich in Astrozyten gebildet und sezerniert. Bereits hier zeigen sich Unterschiede zwischen den ApoE2/3 und der ApoE4-Isoform(en): Letztere wird weniger stark sezerniert, und schneller abgebaut. ApoE4 führt zu verstärkter Neuroinflammation (z.B. durch Erhöhung der Tumour Necrosis Factor alpha (TNF-a) in Mikrogliazellen, zu verminderter Aktivierung der guten neuronal lokalisierten Rezeptoren (z.B. ApoE-Rezeptor 2, ApoE-R2, und Low density lipoprotein receptor-related protein 1, LRP1-Rezeptor) und kann weniger Cholesterol ins Neuron und weniger Amyloid-beta aus dem Hirnparenchym in die Blutbahn transportieren. Lipid-Metabolismus Eine sehr wichtige physiologische Funktion von ApoE im Gehirn ist der Transport von Cholesterol in die Nervenzellen, das diese Zellen für das Auswachsen von Axonen, die Bildung von Synapsen und den Umbau der Zelle im Allgemeinen benötigen. Die ApoE4-Isoform kann im Vergleich zu ApoE2 und 3 Cholesterol weniger stark binden und wird von Astrozyten rascher abgebaut. Es wird angenommen, dass sich diese Kombination – „zu wenig und weniger wirksames Transportmittel für Cholesterol“ – nachteilig auf die Entstehung und den Verlauf der Alzheimererkrankung auswirkt [1]. Neuroinflammation
Neuroinflammation ist einerseits eine wichtige Funktion, um das Gehirn vor Keimen zu schützen und Abfallstoffe zu beseitigen, andererseits führt eine zu starke lokale Entzündungsreaktion oft zu direkter Schädigung des betroffenen Hirngewebes. Es wird angenommen, dass eine überschießende Neuroinflammation auch bei der Alzheimererkrankung eine wichtige Rolle spielt. Hier gibt es Hinweise, dass ApoE4 – stärker als ApoE2 oder 3 – pro-inflammatorische bzw. reduzierte anti-inflammatorische Funktionen aufweist [5]. Passend dazu zeigte sich eine Reduktion des Alzheimerrisikos bei Einnahme von entzündungshemmenden Medikamenten (non-steroidal anti-inflammatory drugs, NSAIDs) nur bei APOE4-Trägern, nicht aber bei den Trägern von APOE2 und 3. Einen Überblick über diese Mechanismen gibt Abbildung 2. Therapeutische Aspekte Es gibt eine Vielzahl von therapeutischen Ansätzen, die auf eine Veränderung von klinischen und pathologischen Aspekten der Alzheimererkrankung fokussieren. Wenige jedoch zielen auf eine Modulation der nachteiligen Wirkungen von ApoE4 im engeren Sinne. Hier sind Ansätze, die versuchen, die ApoE4-spezifische Struktur/ Funktion zu verändern (und sie z.B. jener von ApoE2 oder 3 anzunähern), zu erwähnen. So sind inzwischen Moleküle bekannt (z.B. GIND-25, ein Disulfonat, und GIND-105, ein Monosulfoalkyl), die zumindest die Aktivität von ApoE4 der von ApoE3 annähern können [6]. Ein praktischerer und sofort umsetzbarer Ansatz ist körperliche Aktivität: Eine kürzlich veröffentlichte Studie konnte zeigen, dass körperlich aktive APOE4-Träger weniger Amyloid-beta-Ablagerungen aufwiesen als jene, die wenig Fitness betrieben [2]. Auch profitieren APOE4-Träger mit hohem Bildungsstand und wenig kardiovaskulären Risikofaktoren von einem reduzierten Alzheimerrisiko.
Literatur Autorenfoto: Friedhelm Albrecht © Universität Tübingen Foto: © istockphoto.com| DOUGBERRY |
L&M 1 / 2014
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Die Autoren:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |