|
&more
 >
Neues Verständnis über das Immunsystem
>
Neues Verständnis über das Immunsystem
Neues Verständnis über das ImmunsystemSpitzfindig und tollWie sich Kreise doch immer wieder schließen! Der Immunologe Ralph M. Steinman hat 1973 begonnen, über dendritische Zellen zu publizieren, Arbeiten, die ihn nach langen einsamen Wegen – drei Tage nach seinem Ableben – zum diesjährigen Nobelpreis für Medizin führten. Ich selbst hatte meine erste Berührung mit einem Immunologen als junger Neurochemiker, als ich fast zur gleichen Zeit den damaligen Direktor des Basel Institute for Immunology Niels Jerne unter Zähneklappern um Unterstützung bei der Einreichung meiner ersten Publikation bat. Extra von Konstanz mit meinem Doktorvater angereist, wusste ich so gut wie nichts über ihn, nur dass er ein wahnsinnig wichtiger Mann war, was durch die Ausmaße seines Dienstzimmers einschüchternd unterstrichen wurde. Erst viel später wurde mir klar, dass ich dem Vater der Jerne-Theorie begegnet war. Was für ein genialer Trick der adaptiven Immunität: Auch als „clonal selection theory of immunity“ bezeichnet, besagt Jernes Theorie, dass das Immunsystem je eine Zelle bereithält, die genau eine mögliche Fremdstruktur, die den Körper bedrohen könnte (und von solchen Antigenen gibt es natürlich unendlich viele), erkennt und sich genau diese – und keine andere – Zelle nach Antigenerkennung vielfach vermehrt und die Bedrohung dann mit einem massiven Bataillon bekämpft werden kann. Niels Jerne hat 1984 den Nobelpreis erhalten, aber was hat dies alles mit dem diesjährigen zu tun? Sensoren zur Außenwelt – dendritische Zellen lange unbeachtet Nun, die Zellen des Immunsystems haben zu den äußeren oder inneren Oberflächen des Körpers (also Haut, Darm etc.) keinen direkten Zugang. Das heißt, die Antigene aus der Außenwelt müssen während ihres/nach ihrem Eindringen so schnell wie möglich eingefangen, „geangelt“ und mit dem Immunsystem in Kontakt gebracht werden. Sie müssen also den Abwehrzellen zugeführt und präsentiert werden, damit dann die besagte Aktivierung erfolgen kann. Lange Zeit nahm man an, dass dies in der Hauptsache von Makrophagen bewerkstelligt würde. Nur Steinman hat dies seit den frühen 70er-Jahren, also zeitlich in etwa parallel zur Akzeptanz der Jerne-Theorie, nie so richtig geglaubt. Er hat bis in die 90er- Jahre hinein die dendritischen Zellen mehr oder weniger im Alleingang untersucht und nachgewiesen, dass diese morphologisch plastischen Zellen mit ihren langen Ausläufern quasi die Sensoren zur Außenwelt und die Angelhaken für die Antigene darstellen. Mit stachelartigen Fortsätzen können sie sogar tight junctions der Epithelien durchdringen und Fühlung mit den Außenflächen aufnehmen. Sie nehmen die Antigene sofort in sich auf, verschlucken sie richtiggehend und spalten sie zu Peptiden. Danach ziehen die dendritischen Zellen ihre Fortsätze zurück, wandern von der Peripherie zu den lymphatischen Organen (i.A. Lymphknoten oder Milz), reifen aus, produzieren stimulierende Zytokine und präsentieren die Antigenpeptide, an MHC-II gekoppelt (major histocompatibility complex – Personalausweis, der jede Zelle als körpereigen ausweist), den betreffenden Lymphozyten. Damit hat sich der Kreis geschlossen, indem Steinman den wohl effektivsten Mittler zwischen der fremden Außenwelt und dem Immunsystem gefunden hat, sodass nun die Lymphozyten von den dendritischen Zellen – à la Jerne – aktiviert und vermehrt werden können. Dass diese Zellen nicht nur gefährliche Eindringlinge von außen, sondern u.U. auch Tumorzellen dem Immunsystem zur Vernichtung melden können, wurde inzwischen zur Grundlage für eine Tumortherapie, die ironischerweise aber auch nicht verhindern konnte, dass Steinman drei Tage vor Bekanntgabe des Preises (30.09.11) seinem Krebsleiden erlegen ist. Dass man ihm den Preis (er erhält eine Hälfte) entgegen den Statuten dennoch gelassen hat, hat dieser lange auf einsamen Spuren wandelnde Forscher allemal verdient. Erkennung von „Selbst“ und „Nichtselbst“ – die Bedeutung der TLRs Die Geschichte über die zweite Hälfte des Preises an Bruce Beutler und Jules A. Hoffmann ist nicht weniger toll, haben diese beiden Forscher sich doch mit der Wirkweise der so genannten „Toll-like receptors“ (TLRs) bei Mechanismen der angeborenen Immunität (innate immunity) befasst. Hoffmann hat wesentlich zur Aufklärung der Beteiligung der TLRs bei der Immunabwehr bei der Fruchtfliege beigetragen und dabei auch schon auf vergleichbare Signalwege bei Säugern hingewiesen (EMBO J. 1995, 14: 536-45; Cell 1996, 86: 973– 83), während Beutler sich ganz den Säugern zuwandte und nachweisen konnte, dass der TLR4 für die Bindung von bakteriellem Lipopolysaccarid (LPS, oder Endotoxin), also für die gram-negative Infektionsabwehr zuständig ist (Blood Cells Mol Dis. 1998, 24: 340–55; Science 1998, 282: 2085–8). Zudem können diese Signalwege auch die adaptive Immunität mitregulieren und spielen somit eine ganz wesentliche Rolle bei Entzündungs- und Immunreaktionen. In den letzten zehn Jahren hat die Anzahl der Publikationen zu den TLR-vermittelten Signalwegen explosionsartig zugenommen. Bei den toll-Proteinen handelt es sich um eine hoch konservierte Familie von Proteinen im ganzen Tier- und sogar im Pflanzenreich, die für die Erkennung molekularer Signaturen, insbesondere zur Unterscheidung von Selbst und Nichtselbst in Organismen, dienlich sind. Sehr wahrscheinlich haben sie daher den Verlauf der gesamten Evolution maßgeblich getrieben und mitbestimmt. Als Entwicklungsbiologe ist es für mich bemerkenswert, dass diese „tolle“ Story von Tübinger Kollegen am MPI für Entwicklungsbiologie ihren Ausgang nahm, die die Rolle der Proteine toll zusammen mit Cactus und Spätzle (ja, da lacht des Schwaben Herz!) bei der Achsenbestimmung in der Fruchtfliege aufgeklärt haben. Mit den diesjährigen Nobelpreisen für Medizin wurden eminente Arbeiten gewürdigt, die bleibende Meilensteine zum besseren Verständnis sowohl der angeborenen als auch der adaptiven Immunität markieren.
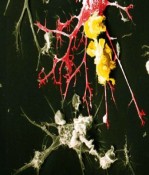
Foto: © Aufnahme MPI für Entwicklungsbiologie Univ. Tübingen, Jürgen Berger; Zellkultur Marion Schneider (Sektion Experimentelle Anästhesiologie, Uniklinik Ulm). http:/ |
L&M 6 / 2011
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |