|
Medizin
 >
Anti Aging
>
Anti Aging
Anti Aging
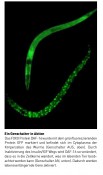
Birgit Holzwarth und Prof. Dr. Ralf Baumeister, Foto: Simone Rethel-Heesters
Wie alle höheren Organismen besteht auch der Mensch aus einer Vielzahl von Zelltypen mit unterschiedlichen Funktionen. Alterungsmechanismen steuern dabei entweder die Zahl der möglichen Teilungen, oder, wie bei den Nervenzellen, die Lebensdauer während der inzwischen durchschnittlich mehr als 80 Jahre lebenden Menschen. Faktoren wie Umweltbedingungen, Lebensgewohnheiten, Ernährungsverhalten und Stressbewältigung scheinen von außen auf die zellulären Prozesse einzuwirken. Verschiedene genetische Mechanismen wurden in den vergangenen Jahren entdeckt und ihre regulatorischen Einflüsse auf die Zellalterung werden inzwischen in Hunderten von Laboratorien untersucht. Seit Cynthia Kenyon von der University of California in San Francisco im Jahr 1993 in einer spektakulären Studie gezeigt hat, dass sich das Leben von Fadenwürmern durch eine einzige Mutation verdoppeln lässt, hat sich der gerade 1 mm große Fadenwurm Caenorhabditis elegans zu einem der bevorzugten Alternsmodelle der Molekularwissenschaften entwickelt. Über 60 % der Gene in C. elegans sind homolog zu den entsprechenden Faktoren des Menschen. Und zahlreiche der bisher untersuchten Gene in C. elegans, die auch auch im menschlichen Genom präsent sind, scheinen dort auch sehr ähnliche Aufgaben zu haben. Perfekte Voraussetzungen, wie wir meinen, um die elementaren Vorgänge des Alterns in dem leicht zu manipulierenden Tiermodell C. elegans zu erforschen und zu verstehen. Die Insulin-Antwort im Alterungsprozess Signalmoleküle wie das Insulin und insulinähnliche Wachstumsfaktoren (IGF) nehmen im Alterungsprozess eine Schlüsselstellung ein. Sie aktivieren und steuern ganze Genkaskaden. Aber – je nach Menge, Angebot und Zeitpunkt der Expression von Insulin/IGF im betrachteten Organismus – können die Folgen entweder fatal oder aber lebensverlängernd sein. Bindet Insulin/IGF an seinen zellulären Rezeptor, so werden dessen Proteinkinase-Domänen im Cytoplasma aktiviert und führen unter Beteiligung von Phosphoinositid- 3-Kinase PI3K zur Phosphorylierung der Serin-/ Threonin-Kinasen AKT-1 und -2. Die Substrate dieser Kinasen sind nun selbst befähigt Zielproteine zu phosphorylieren und nehmen damit Einfluss auf die Expression von Zielgenen, die die Lebensdauer der Zelle maßgeblich beeinflussen können. Einer der entscheidenden Faktoren dabei ist der FOXO-Transkriptionsfaktor DAF-16, der durch Phosphorylierung inaktiviert und im Cytoplasma festgehalten wird. Reduktion des Insulinsignals verhindert diese Modifiaktion und führt zu dessen Wanderung in den Zellkern, wo er eine Vielzahl protektiver Gene reguliert. Vor einigen Jahren konnten wir zeigen, dass die FOXO-Phosphorylierung wesentlich von der Aktivität eines weiteren Gens namens sgk-1 abhängt. sgk-1 kodiert für die Serum- und Glukokortikoid- induzierbare Proteinkinase und bildet mit den AKTKinasen einen Enzymkomplex in der Zelle, dessen einzelne Komponenten unterschiedliche Aufbagen zu haben scheinen. Insulin und oxidativer Stress – Gegenspieler im Alterungsprozess ? Je nach Aktivierung von FOXO/DAF-16 werden unterschiedliche Zielgene im Zellkern in Gang gesetzt. Diese sind unter anderem an der Regulation des Zellzyklus, am Schutz vor reaktiven Sauerstoffspezies (ROS), der Reparatur der Zelle, der Apoptose und einer Reihe von metabolischen Funktionen (im Stoffwechsel) beteiligt. Neben AKT und SGK-1 wirken eine ganze Reihe weiterer Proteine auf die FOXO/DAF-16 Aktivität. Besonders intensiv werden dabei die Enzyme der Sir2-Familie (Sirtuine) untersucht, Deacetylasen, deren Aktivität durch Resveratrol, einen Bestandteil von Weintrauben (und Rotwein), verändert werden kann. Stresseinflüsse aktivieren auch mehrere MAP-Kinase-Signalwege, die parallel zum Insulin wirken und wie die Jun Kinase JNK-1 ebenfalls über Phosphorylierungen auf die FOXO-Aktivität einwirken. Ein entscheidendes Bindeglied zwischen Insulin und JNK-Wegen stellt dabei ein Adapter namens SHC dar, der, wie wir erst ganz kürzlich zeigen konnten, für die lebensverlängernden Programme der Zelle unbedingt gebraucht wird. Wie aber nun funktioniert die lebensverlängernde Aktivierung von FOXO/DAF-16? Über hunder Gene, deren Expression von DAF-16 gesteuert wird, wurde inzwischen entdeckt. Viele der Mutanten, die die Aktivität des Insulinwegs unter bestimmten Bedingungen reduzieren, betreffen Gene, die die zelluläre Resistenz gegen die schädlichen Einflüsse von Sauerstoffradikalen reduzieren. Mit der verbesserten Widerstandskraft gegen Radikale verlängert sich auch die Lebenserwartung der Fadenwürmer. Und tatsächlich zeigen Studien in Familien mit überdurchschnittlich häufigem Aufkommen von Hundertjährigen, dass auch bei diesen der Insulin-/IGF- Signalweg deutlich niedrigere Aktivität zeigt. Somit scheinen diese Mechanismen zwischen Wurm und Mensch überraschend ähnlich zu funktionieren. Insulin regelt einen der wichtigsten Stressregulatoren In Zusammenarbeit mit Keith Blackwells Gruppe am Joslin Diabetes Center der Harvard Medical School gelang es uns kürzlich, eine weitere bedeutende Funktion des Insulinwegs zu entdecken. Dieser steuert demnach auch die Funktion des Transkriptionsfaktor SKN-1/Nrf2, eines schon länger bekannten Schlüsselregulators der Stressabwehr. Jedoch war man bislang davon ausgegangen, dass SKN-1/Nrf2 ausschließlich über MAP-Kinasen, nicht aber über Insulin, gesteuert wird. In unseren jüngsten Forschungsarbeiten an C. elegans fanden wir heraus, dass im Verdauungstrakt von C. elegans eine Reduktion der Insulin-Signalkaskade ebenfalls ausreicht, um den Transport von SKN-1 vom Cytoplasma in den Zellkern auszulösen und dadurch das Phase IIDetoxifikationsystem zur Abwehr von Sauerstoffradikalen in den Mitochondrien zu kontrollieren und zu aktivieren. Letzteres stellt eines der wichtigsten genetischen Netzwerke zum Schutz der Zelle bei oxidativem Stress dar. Lebensqualität und Lebenserwartung
Das Zusammenspiel unterschiedlicher Signalwege erscheint mit zunehmender Forschung immer komplexer, wird aber auch immer besser verstanden. Durch die Erkenntnisse der Systembiologie, einer neuen interdisziplinär agierenden Forschungsrichtung in den Naturwissenschaften, versucht man nun die Dynamik dieses komplexen Netzwerks mit inzwischen über 150 bekannten Faktoren in allen Einzelheiten zu verstehen und durch mathematische Modelle vorherzusagen. Sie könnten in Zukunft dazu beitragen, die Wirkung von verabreichten Medikamenten im Einzelfall präziser vorherzusagen, als dies jemals durch Untersuchungen ein zelner Regulatoren oder Signalbausteine möglich wäre. Ziel dieser Untersuchungen ist dabei auch, die genetischen Konsequenzen alternder Zellen zu verstehen und ihre Einflüsse auf die Aktivität lebenserhaltender Enzyme kennenzulernen. Ziel solcher Anti-Aging-Forschung ist es dabei weniger, das Leben eines Fadenwurms zu verlängern, als vielmehr Kenntnis für die Funktion der betreffenden menschlichen Gene und Proteine zu erhalten. Dies könnte dann der Früherkennung und vielleicht eines Tages der Behandlung all derer Krankheiten zugute kommen, deren Hauptrisikofaktor das Altern ist. Und auch für die Wirkstoffsuche gegen Alzheimer, Parkinson und Krebs hat sich C. elegans in der Vergangenheit bereits als hervorragend geeignet erwiesen.
Foto 1: © Simone Rethel-Heesters |
L&M 5 / 2008
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Die Autoren:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |