|
Medizin
 >
Potenzial der Glykomik für die Therapie menschlicher Krankheiten
>
Potenzial der Glykomik für die Therapie menschlicher Krankheiten
Potenzial der Glykomik für die Therapie menschlicher Krankheiten
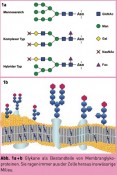
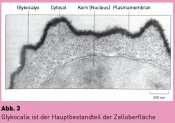
Prof. Dr. Werner Reutter, Institut für Biochemie und Molekularbiologie, Charité Campus Benjamin Franklin Verschiedene biologische und glykobiotechnologische Ziele bieten sich aufgrund ihres Vorkommens in Oberflächen von Proteinen oder Zellen an (Abb. 2). Auf vier Beispiele soll näher eingegangen werden. Auffinden von Inhibitoren der Biosynthese Alle Zellen sind von einer Zuckerschicht, der Glykokalix, umgeben, einem komplexen Netzwerk aus Glykoproteinen und Glykolipiden, deren Zuckeranteil aus der Zelloberfläche herausragt (Abb. 3). Die Glykokalix verleiht der Zelloberfläche einen Schutz nach außen. Sie legt sich wie eine Tarnkappe um die Zelle und verhindert den Kontakt mit Proteinen und Lipiden der eigenen Zelloberfläche oder die Erkennung durch Zellen des Immunsystems (Lymphozyten). Findet die Erkennung von Membranproteinen trotzdem statt, reagiert der Organismus mit der Bildung von Antikörpern gegen die eigenen Zellen, wie es bei Autoaggressionskrankheiten geschieht. Tumorzellen zeichnen sich im Besonderen durch eine spezifische Modifikation der Tarnkappe aus, durch eine verstärkte Ausstattung mit N-Acetylneuraminsäure, auch Sialinsäure benannt. Diese Zuckersäure ist für die Verhinderung der Erkennung von Zellen der körpereigenen Abwehr in besonderer Weise verantwortlich, wenn sie im Übermaß aus der Zelloberfläche herausragt. Daher ist die Auffindung von Inhibitoren der Biosynthese der N- Acetylneuraminsäure bzw. ihre Anheftung an Glykoproteine der Zelloberfläche ein vordringliches Ziel. Erste Erfolge konnten bereits durch die Synthese von in vitro wirksamen Inhibitoren erzielt werden. Regulation von Entzündungsprozessen
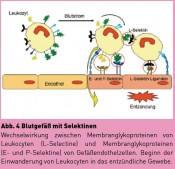
Entzündungsprozesse werden von Zuckern von Zelloberflächenkomponenten, den Selektinen, reguliert. Um entzündungsverursachende Fremdsubstanzen zu bekämpfen, müssen die verantwortlichen weißen Blutzellen (Granulozyten) aus dem Blutstrom in das geschädigte Gewebe gelangen. Dazu interagieren Zuckerketten von Selektinen der Granulozytenoberfläche mit dazu passenden Glykanen der Gefäßendothelien (Abb. 4). Diese Wechselwirkung ist der Beginn der Evasion von Granulozyten aus dem Blutstrom in das geschädigte Gewebe. Das Überschießen eines Entzündungsprozesses soll durch Substanzen gehemmt werden, die sich zwischen die interagierenden Zuckerketten lagern und so das weitere Eindringen von Granulocytenin in das Gewebe unterdrücken. Dieses Gebiet befindet sich ebenfalls in einem vielversprechenden Anfang. Entwicklung spezifischer Enzyminhibitoren Eine weitere Bedeutung der N-Acetylneuraminsäure der Zelloberfläche ist bei einer der häufigsten Infektionskrankheiten gegeben, der Grippe. Sie wird durch Influenza- A-Viren mit ihren verschiedenen Unterformen HxNy (x, y = 1 bis 5) hervorgerufen. Das berüchtigte H5N1-Virus führt zur Vogelgrippe. Die viruseigene Neuraminidase oder Sialidase ist für das Eindringen des Virus in die Zelle unerlässlich. Die erfolgreiche Behandlung der Frühform von Influenza-A-Infektionen gelingt neuerdings durch den Einsatz der Sialidasehemmer Relenza (intranasale Applikation) und Tamiflu (systemisch). Die Entwicklung dieser spezifischen Enzyminhibitoren war ein Meilenstein der modernen Glykobiotechnologie. Ein anderes Beispiel ist die Chagaskrankheit – eine durch Parasiten hervorgerufene in Südamerika sehr häufige Krankheit. Auch bei ihr spielt Neuraminsäure eine herausragende Rolle. Chagas-Patienten sterben nach der Infektion mit Trypanosoma cruzi meist an einem Herzversagen. Sein Parasitendasein zeigt T. cruzi durch die Einverleibung der Wirts-Neuraminsäure/Sialinsäure durch Vermittlung einer Transsialidase auf seiner Oberfläche. Sie spaltet vom Wirt, dem Menschen, Neuraminsäure ab und überträgt sie mit dem gleichen Enzymmolekül auf seine Oberfläche und schützt sich so vor dem Immunsystem des Befallenen („Tarnkappe“). Auch hier ist die Suche nach Enzyminhibitoren im Gange. Die Schutzwirkung der Sialinsäure ist für die Verweilzeit im Blut für eine Reihe therapeutisch angewandter Glykoproteine bedeutsam. Das gilt für rekombinante Wachstumsfaktoren, die bei der Behandlung der Anämien von Tumorpatienten oder Dialysepatienten das blutbildungsstimulierende Erythropoietin benötigen, für Bluter Gerinnungsfaktoren brauchen, bei MS- und Tumorpatienten, die mit Interferonen behandelt werden, um nur einige zu nennen. Hauptvertreter in dieser Gruppe der wachstumsstimulierenden rekombinanten Glykoproteine ist Erythropoietin (EPO), das die Produktion von roten Blutkörperchen anregt. Seine relativ kurze Halblebenszeit im Blut wurde gentechnologisch verlängert, indem zusätzliche Glykosylierungsstellen in das Molekül eingebracht wurden. Dadurch wurde im EPOMolekül die Zahl der Glykanketten mit ihren schützenden Sialinsäuren vergrößert. Gentechnologische Modifikationen werden auch an Antikörpern vorgenommen, um sie biologisch stabiler zu machen. Mit Hilfe eines neuen glycobiotechnologischen Verfahrens ist es möglich geworden, N-Acetylneuraminsäure so zu verändern, dass sie sich im Verbund von Glykanen gegenüber Neuraminidasen resistenter zeigen. Dazu wurde die physiologische N-Acetylseitenkette nur geringfügig modifiziert, sie wurde um eine Methylen (-CH2-) gruppe verlängert. Dazu wurde einfach der natürliche biochemische Vorläufer der Sialinsäure, N-Acetylmannosamin, durch N-Propionyl-mannosamin (oder homologe Analoga) ersetzt. Damit ist eine chancenreiche Möglichkeit gegeben, die biologische Stabilität rekombinanter Glykoproteine deutlich zu erhöhen. Entwicklung von Impfstoffen Dem Arbeitskreis von P. Seeberger ist es gelungen, die hoch komplizierte Synthese von Zuckerketten entscheidend zu vereinfachen und maschinell in relativ kurzer Zeit herzustellen. Neben vielen Vorteilen für Fragestellungen aus der Grundlagenforschung der Glykobiologie ist damit eine Basis für die Entwicklung von Impfstoffen geschaffen worden. Sie betreffen bakterielle und parasitäre Krankheiten, bei denen das toxische Agens in typischen Zuckerstrukturen der Mikrobe liegt, z. B. bei der Malaria und anderen Tropenkrankheiten. Sie betreffen aber auch bestimmte Krebserkrankungen wie das maligne Melanom. Das Potenzial dieses neuen glykotechnologischen Vorgehens ist sehr groß. Erfolgreiche Wege in der Medizin Nur erwähnt seien hier Heparin und seine Abkömmlinge, die ersten Glycan-basierten Therapeutika, die zu den Top Ten der Arzneimittel gehören und als Antikoagulantien seit den 30er Jahren die Verklumpung von roten Blutkörperchen verhindern. Die Pharmaindustrie ist intensiv bemüht, neue niedermolekulare, nebenwirkungsfreie Formen des Heparins mit antithrombotischer Aktivität zu synthetisieren. Weiterhin sei hier das Monosaccharid D-Galactose bei Demenzpatienten erwähnt, das als Nahrungsergänzungsmittel bei Alzheimer-Patienten und Patienten mit Foto: © Prof. Dr. Werner Reutter |
L&M 5 / 2008
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |