|
Medizin
 >
Infektionsforschung mit Glycochips
>
Infektionsforschung mit Glycochips
Infektionsforschung mit GlycochipsDem Zuckercode auf der Spur
Dr. Jürgen Seibel und Lars Hillringhaus, Helmholtz-Zentrum für Infektionsforschung, Braunschweig Ob Virusinfektionen, wie die Vogelgrippe H5N1 und HIV, Krebs oder Malaria – Zuckerverbindungen spielen bei einer ganzen Reihe von Krankheiten eine entscheidende Rolle. Um jedoch ihre genaue Funktion herauszufinden und etwa für die Entwicklung von Impfstoffen zu nutzen, müssen Forscher die wichtigsten Zuckerverbindungen aufspüren und im Labor nachbauen. Seit kurzem wurde dafür ein passendes Werkzeug entwickelt: der Glycochip. Mit ihm lassen sich nicht nur spezielle Zuckerverbindungen aufbauen, sondern auch ihre Funktionen und damit mögliche medizinische Anwendungen schnell erkennen. Komplexe Zucker, sogenannte Oligosaccharide, sind in den Fokus der aktuellen Forschung gelangt. So ist die menschliche Zelle von Zuckern ummantelt. Dort beeinflussen sie zahlreiche biologische Prozesse. Sie entscheiden beispielsweise darüber, ob ein fremder Stoff ins Innere einer Zelle gelassen wird oder nicht. Ebenso verläuft die Erkennung von Grippeviren über Zucker auf Zelloberflächen, woraufhin sich die Viren in menschlichen Zellen vermehren können. Des Weiteren charakterisieren Zucker den Zustand einer Zelle. Tumorzellen sind von anderen Zuckern ummantelt als gesunde Zellen und bieten somit die Möglichkeit und Perspektive, mit Zuckerimpfstoffen die menschliche Immunabwehr auf Tumorzellen auszurichten. Die Erforschung des Zuckercodes
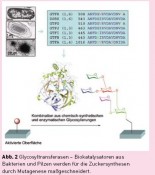
Oligosaccharide bestehen aus einzelnen Zucker-Bausteinen (Monosaccharide), die auf unterschiedliche Weisemiteinander verknüpft werden können. Wie bei anderen Biomolekülen dient die Art ihrer Verknüpfung der Speicherung von Informationen. Während Gene und Proteine nur linear miteinander verknüpft werden können, sind bei Zuckern auch Verzweigungen in 8 verschiedene Richtungen möglich. So ergibt sich eine enorme strukturelle Vielfalt, die Proteine nutzen, um die in Zuckern gespeicherte Information abzulesen. Über diesen sogenannten Zuckercode ist bis jetzt jedoch noch viel zu wenig bekannt. Will man den „Zuckercode“ entschlüsseln bzw. verstehen, benötigt man entsprechende Mengen der auf den Zellen vorkommenden Zucker. Diese können aber nicht einfach isoliert werden, da sie einerseits nur in sehr geringen Mengen und andererseits in vielen verschiedenen Formen vorkommen, die sich nicht voneinander trennen lassen. Daher müssen die Zucker möglichst synthetisch hergestellt werden. In unserem Körper werden einzelne Zuckerbausteinen miteinander zu komplexen Oligosacchariden durch spezielle Enzyme, sogenannte Glycosyltransferasen, aufgebaut. Die Synthese im Labor ist da weitaus komplizierter: Häufig können bestimmte Zucker nur chemisch synthetisiert werden, was in der Regel aufwändiger Synthesen bedarf, die unter Einsatz von Schwermetallen und enormem Zeitaufwand erfolgen. Zucker werden folglich nur selten in therapeutischen Maßnahmen eingesetzt, da ihre kostengünstige Produktion aufgrund des hohen synthetischen Aufwands versperrt ist. Hier setzt die Arbeitsgruppe um Jürgen Seibel an. Sie nutzt beispielsweise Enzyme, die normalen Haushaltszucker anstelle der speziellen Bausteine umsetzen können. Diese Enzyme stammen nicht aus menschlichen Zellen, sondern aus Bakterien und Pilzen [1]. Allerdings sind die Enzyme sehr selektiv, sie können deshalb nicht jede beliebige Verknüpfung einzelner Zuckerbausteine durchführen. Deshalb wurden ihre natürlichen Synthese-Eigenschaften im Labor erweitert. Durch Mutagenese der Glycosyltransferase-Gene wurden Enzymbibliotheken generiert und auf neue Eigenschaften getrimmt. So können die Enzyme auf die jeweilige Anwendung maßgeschneidert werden [2]. Durch eine zielgerichtete Kombination von Zuckerbausteinmodifikation (Substrat-Engineering) und Katalysatordesign (Enzym-Engineering) können die Synthesemöglichkeiten komplexer Zucker nun enorm erweitert werden [3, 4]. Analyse auf dem Glyco-Chip
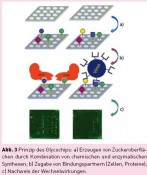
Mithilfe dieser modernen Synthesemethoden lassen sich Bibliotheken von Zuckern erhalten, welche bei zellulären Prozessen von Bedeutung sein können. Doch wie kann man sie möglichst schnell auf ihre biologischen Funktionen hin testen? Hierfür haben sich die Helmholtz-Forscher an einem Werkzeug der Genforscher orientiert: Diese verwenden seit geraumer Zeit kleine Glas-Chips, mit denen untersucht werden kann, wie stark Gene in bestimmten Zellen abgelesen werden (Genotyping), sogenannte DNA-Arrays. Dieses System konnte vor wenigen Jahren auf Zucker übertragen werden. Die Glyco- Chips (auch als Glyco-Arrays bezeichnet) bestehen aus auf Polyacrylamid-beschichteten Glas-Slides gespotteten Oligosacchariden. Diese wurden entweder rein chemisch oder mithilfe von Enzymen auf den Chips kovalent, also fest, aufgebaut (siehe Abbildung) [5]. Auf dem Chip sind nur minimalste Mengen an Zuckern erforderlich, wodurch die Limitierung aufgrund schwieriger Synthesen als auch die Umweltbelastung aufwändiger Synthesen enorm reduziert wird. Die Glasoberfläche ähnelt somit der Oberfläche einer Zelle, auf der die Kohlenhydrate wie Antennen abstehen, um Signale an die Zelle weiterzuleiten. Nach der Anbindung der Zucker auf die Glasoberfläche werden farbstoffmarkierte Proteine zugegeben und anschließend die Oberfläche mit Wasser gespült. Nicht gebundene Proteine werden dadurch von der Oberfläche abgewaschen. Proteine hingegen, welche bestimmte Zucker auf dem Glas-Chip erkennen, bleiben auch beim Spülen gebunden und können durch ihren Farbstoff als ein fluoreszierender Spot mithilfe eines Scanners nachgewiesen werden. So erhält man Informationen darüber, welche Proteine an welche Kohlenhydrate binden und welche Moleküle die Bindungsprozesse verstärken bzw. unterbinden können. Die Lichtintensität der leuchtenden Punkte gibt Aufschluss, wie gut ein Protein bestimmte Zucker erkennt. Doch nicht nur Proteine können auf dem Chip untersucht werden. Es kann auch menschliches Serum auf den Chip gegeben werden. Hierbei binden Antikörper, welche das menschliche Immunsystem produziert hat, an bestimmte Kohlenhydrate. Dies bietet die Möglichkeit, Krankheiten wie Krebs bereits im Frühstudium nachzuweisen. Therapien, welche im Frühstadium von Krankheiten durchgeführt werden, sind in der Regel viel erfolgversprechender als solche, die erst in einem fortgeschrittenen Stadium der Krankheit begonnen werden. Der Nachweis bestimmter Zucker ist sogar auf ganzen Zellen möglich. Hierbei werden die gesuchten Zucker derart modifiziert, dass Farbstoffe an sie gebunden werden können. Die Zellen, welche den gesuchten Zucker auf ihrer Oberfläche tragen, sind dann durch leuchtende Punkte an ihren Oberflächen sichtbar. Somit können etwa Tumorzellen sichtbar gemacht werden, da diese spezielle Zucker auf ihrer Oberfläche haben. Perspektiven Die Erforschung von Zuckern hat durch die Entwicklung neuer Synthesemethoden einen großen Aufschwung bekommen. Mithilfe kleiner Glas-Chips können in kürzester Zeit eine Vielzahl von Wechselwirkungen untersucht werden, welche der Entschlüsselung des Zuckercodes zur Entwicklung von Medikamenten gegen Infektionskrankheiten und Krebs dienen. Glycochips sind zudem ein vielversprechendes Werkzeug zum Auffinden von Biomarkern für zahlreiche Krankheiten. Möglicherweise können Glycochips in Zukunft in Kliniken dem schnellen Nachweis von Krankheiten und Therapiemöglichkeiten dienen. Foto: © Dr. Jürgen Seibel
Literatur |
L&M 5 / 2008
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |