|
Forscher
>
Prof. Dr. Manfred Grote
>
Antibiotikarückstände aus der Landwirtschaft – Beiträge zur Resistenzentwicklung
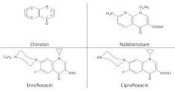
Antibiotikarückstände aus der Landwirtschaft – Beiträge zur ResistenzentwicklungResistente Keime in Fleisch und Gemüse?In den beiden letzten Jahrzehnten wird weltweit eine drastische Zunahme an antibiotikaresistenten pathogenen Keimen beobachtet. Ein Großteil der traditionellen Antibiotika ist dadurch zur Behandlung von Infektionen bei Mensch und Tier unwirksam geworden. Für das Gesundheitswesen ist damit ein ernsthaftes Problem entstanden: Infektionen, die von multiresistenten Bakterien verursacht werden, sind schwierig zu therapieren, verlängern die Behandlungsdauer und führen zu einer erhöhten Mortalität sowie zu höheren Behandlungskosten [1]. Die Entwicklung und Ausbreitung resistenter humanpathogener Erreger wird ursächlich u.a. mit dem extensiven Antibiotikaeinsatz in der Massentier haltung in Verbindung gebracht. Frühe Warnungen: Anwendung derselben Antibiotika für Mensch und Tier „Es muss vermieden werden, durch Antibiotikabehandlung unterschwellige Dosen in den menschlichen oder tierischen Körper gelangen zu lassen …, es muss bis zur Klärung aller Fragen Zurückhaltung geübt werden.“ Diese Forderung wurde bereits im Jahre 1960 von H. Köhler [2] erhoben, die Studien über die Anwendung von Antibiotika im Pflanzenschutz durchgeführt hatte und dabei die Problematik antibiotikaresistenter pathogener Keime erkannte. Auf „Zurückhaltung“ kann nicht geschlossen werden, da Antibiotika in der Folgezeit bis heute sowohl in der Humanmedizin als auch in der Veterinärmedizin zu den verordnungsstärksten Indikationsgruppen zählen. Im Jahre 1969 empfahlen britische Wissenschaftler im so genannten Swann-Report, hochwirksame Wirkstoffe auf den Einsatz für den Menschen zu beschränken und die Freigabe für die tiermedizinische Anwendung restriktiv zu handhaben – auch diese als „zu zaghaft“ eingeschätzte Empfehlung fand nicht genügend Beachtung. Wirkungslos blieb ebenso die Entdeckung, dass 1990, also nur 2 Jahre nach Zulassung des Enrofloxacins (ein Fluorchinolon) für tiermedizinische Anwendungen, 13 % der Salmonellenproben gegen humanmedizinisch applizierte Chinolone (Nalidixinsäure) resistent waren (Abb. 1). Von daher ist es keine Überraschung, dass bereits nach einem Jahr chinolonresistente Keime sowohl bei Tieren, in Lebensmitteln, in der Umwelt als auch in Kliniken nachgewiesen wurden. Da sich in der Folgezeit in den USA bei Klinikpatienten und Heimbewohnern die Anzahl nicht therapierbarer Salmonellainfektionen drastisch erhöht hatte, wurde aufgrund der rasanten Resistenzentwicklung im Jahre 2005 die Anwendung von Enrofloxacin in der Geflügelzucht verboten. Ungenügend erhitzte, mit resistenten Keimen belastete Geflügelgerichte waren die Quelle dieses Ausbruchs. Eine aktuelle Studie des nordrhein-westfälischen Landesamtes für Natur, Umwelt und Verbraucherschutz (LANUV-NRW) enthüllte, dass bei der Hähnchenmast in 83 % der Mastdurchgänge antibiotisch wirksame Medikamente eingesetzt werden – darunter auch Chinolone [3]. Multiresistente Keime: MRSA, ESBL – Zoonosen
Seit den 1990er-Jahren weisen Staphylokokkenstämme mit zunehmender Tendenz Multiresistenzen gegenüber allen wichtigen Antibiotikaklassen wie Fluorchinolone, Sulfonamide, Tetracycline und Beta-Lactame (z.B. Penicilline, Amoxicillin) auf. Als Konsequenz steigt drastisch die Anzahl schwerer Infektionen durch methicillinresistente Stämme des Staphylococcus aureus (MRSA; Methicillin ist chemisch verwandt mit Penicillin), wovon besonders Knochen, Haut und Wunden betroffen sind. Nach aktuellen Angaben der Weltgesundheitsorganisation WHO sterben jedes Jahr in Europa ca. 25.000 Menschen an einer Infektion mit multiresistenten Bakterien. In den USA wurden etwa 18.600 Todesfälle im Jahr 2005 auf eine MRSA-Infektion zurückgeführt – das sind mehr Todesfälle als durch Aids. Besorgniserregend ist auch die Zunahme antibiotikaresistenter pathogener Enterobakterien (Enterobacteriaceae). Nichtpathogene Stämme dieser Bakteriengruppe sind Bestandteil der Darmflora von Mensch und Tier wie Escherichia coli (E. coli) und Salmonellenstämme (Salmonella enterica). Aber einige dieser Keime tragen pathogene Eigenschaften, die in Boden, Wasser und in Nahrungsmitteln tierischen und pflanzlichen Ursprungs auftreten können. Sie verursachen zunehmend Infektionen, die in besonderem Maße für Frühgeborene und immungeschwächte Patienten gefährlich Industrielle Tierproduktion: eine Quelle für Antibiotikarückstände und resistente Keime Lange Zeit wurde ein Zusammenhang zwischen dem Antibiotikaeinsatz in der Landwirtschaft und der Entstehung und Verbreitung resistenter humanpathogener Mikroorganismen nicht erkannt – oder er wurde und wird noch bestritten! Im Fokus steht dabei die intensive Nutztierhaltung („industrielle Tierproduktion“), insbesondere die von Schwein und Geflügel. Nach Schätzungen liegt die Anwendungsmenge von Veterinärantibiotika in Deutschland für das Jahr 2005 zwischen ca. 800 und 2100 Tonnen (Zum Vergleich: Für die Humanmedizin wurden im Jahr 2004 ca. 1600 Tonnen Antibiotika eingesetzt.). Zuverlässige aktuelle Verbrauchsdaten sind gegenwärtig nicht verfügbar. Mit einem Anteil von ca. 44,6 % erreichen Tetracycline, die für Schwein, Rind und Geflügel eingesetzt werden, die höchsten Verkaufszahlen, gefolgt von Beta-Lactamen (25,4 %), Sulfonamiden (12,4 %) und Makroliden (6,7 %). Deutlich niedriger ist der Verbrauch an Fluorchinolonen mit nur 1 %. Anwendungsbereiche für Veterinärantibiotika Seit Januar 2006 besteht das EU-weite Verbot, Antibiotika bei der intensiven Tierhaltung dem Futter in geringen „subtherapeutischen“ Mengen (< 100 mg/kg Futter, abhängig vom Wirkstoff) zuzugeben. Diese Zusätze dienten der sog. „Leistungsförderung“, d.h. einer verbesserten Futterverwertung bei der Produktion von Geflügel-, Rind- und Schweinefleisch. Ein geringerer Futterverbrauch pro Kilogramm Gewichtszuwachs des Tieres und ein schnelleres Erreichen des Schlachtgewichtes mit niedrigeren Kosten für Futtermittel waren die Folge – aber auch eine bedrohliche Zunahme an resistenten humanpathogenen Keimen. Daher dürfen seit dem 1. Januar 2006 Veterinärantibiotika nur noch nach tierärztlicher Verschreibung auf Grundlage des Arzneimittelrechtes zur Therapie von Infektionskrankheiten und prophylaktisch bei chirurgischen Maßnahmen angewendet werden – aber ebenso zur „Metaphylaxe“. Das bedeutet, dass bei der Erkrankung nur weniger Tiere eines Stalles der gesamte Tierbesatz mit Antibiotika versorgt werden kann – und dass Geflügelfarmer für mehrere zehntausend Hühner das Trinkwasser mit antibiotischen Wirkstoffen „metaphylaktisch“ versetzen. Diese Praxis spiegelt sich in den oben erwähnten Daten der LANUV-Studie zum hohen Antibiotikaeinsatz in der Geflügelmast wider. Transfer Boden – Pflanze: Antibiotika und Keime
In Deutschland fallen jährlich ca. 30 Mio. Tonnen an tierischen Exkrementen an, überwiegend Schweinegülle, besonders regional in viehstarken Gebieten. Über die Gülle, genutzt als Wirtschaftsdünger, gelangen die von den Tieren nach Applikation ausgeschiedenen Antibiotikawirkstoffe und ihre Metaboliten auf landwirtschaftlich FAZIT – Deutsche Antibiotika- Resistenzstrategie DART
In dem vom Bundesamt für Verbraucherschutz und Lebensmittelsicherheit (BVL) u.a. herausgegebenen Bericht GERMAP 2008 [10] werden sowohl der Antibiotikaverbrauch als auch die Verbreitung von Resistenzen in der Human- und Veterinärmedizin der letzten Jahre in Deutschland dargestellt. Es zeigt sich, dass die zur Verfügung stehende Datenbasis zu gering ist, um verlässliche Risikoabschätzungen im Rahmen eines vorsorgenden Verbraucherschutzes zu ermöglichen. Mit der Deutschen Antibiotika-Resistenzstrategie DART [1] veröffentlichte die Bundesregierung im November 2008 ein Konzept, dessen zentrales Ziel die Reduzierung der Bildung und Ausbreitung von Antibiotikaresistenzen in Deutschland ist. Als Konsequenz aus den beschriebenen rückstandsanalytischen und mikrobiologischen Befunden sowie der zunehmenden Brisanz der Resistenzlage sind Strategien und interdisziplinäre Forschungsansätze zu entwickeln, die zu einem nachhaltigeren Einsatz von Veterinärantibiotika in der Landwirtschaft führen, mit dem Ziel der Resistenzprävention. Das vom BMBF geförderte interdisziplinäre Verbundprojekt RESET („ESBL and (fluoro)quinolone Resistance in Enterobacteriaceae“, www.reset- Literatur
[1] BMG, Bundesministerium für Gesundheit (Hrsg.) (11/2008): DART – Deutsche Antibiotika-Resistenzstrategie. BMG-G-07014, Berlin 2011. Foto: © Prof. Dr. Manfred Grote |
L&M 2 / 2012
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:NewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |